某校学生化学实验小组,为验证Cl2氧化性强于硫和N2,设计了一套实验装置:
(部分夹持装置已略去)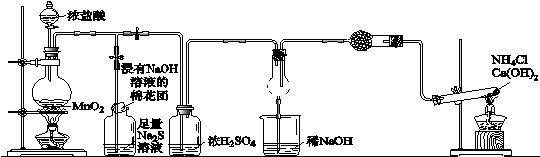
A B C D E
(1)写出A中反应的离子方程式
(2)B中出现黄色浑浊现象,产生此现象的离子方程式
(3)D中干燥管中出现的现象为
产生的NH3过量,则D干燥管发生化学方程式为
(4)有同学认为D中的现象并不能说明Cl2氧化性强于N2,需要在C之前加装洗气装置,请画出
其装置图 (并注明盛装试剂)。
(5)证明非金属性Cl > S,用另一种相关事实说明
氯化亚铜(CuCl)是白色粉末,不溶于水、乙醇及稀硫酸,熔点422℃,沸点1366,在空气中迅速被氧化成绿色,常用作有机合成工业中的催化剂。以粗盐水(含Ca2+、Mg2+、SO42-等杂质、Cu、稀硫酸、SO2等为原料合成CuCl的工艺如下:
(1)A的化学式为。
(2)写出反应V的化学方程式。
(3)写出反应VI的离子方程式为。
(4)本工艺中可以循环利用的物质是(刚化学式表示)。
(5)反应VI后,过滤得到CuCl沉淀,用无水乙醇洗涤沉淀,在真空干燥机内于70℃干燥2小时,冷却,密封包装即得产品。于70℃真空干燥的目的是。
(1)铝是一种重要的金属材料,铝热反应可以焊接钢轨,请写出铝在高温下与三氧化二铁反应的化学方程式
(2)某铝合金中含有合金元素镁、铜、硅,为了测定合金中铝的含量,设计了如下实验,请回答有关问题:
①称取样品ag,将样品溶于足量的稀盐酸,过滤;
②滤液中加入过量的氢氧化钠溶液,过滤,有关的离子方程式为:
③步骤②的滤液中通过足量的CO2气体,可产生Al(OH)3沉淀
④步骤③过滤后的滤渣用蒸馏水洗涤数次,烘干并灼烧至恒重,冷却后称量,其质量为bg,原样品中铝的质量分数为
(3)工业上,硅是在电炉中用炭粉还原二氧化碳硅制得的,写出该反应的化学方程式
,若往电炉中加入12g二氧化硅和足量炭粉的混合物,生成的气体在标准状况下的体积为。
化学电池在通讯、交通及日常生活中有着广泛的应用。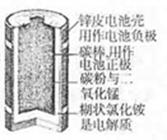
(1)右图是锌锰干电池的基本构造图,关于该电池的使用和性能,说法 正确的是
正确的是
A.该 电池可充电后反复使用
电池可充电后反复使用
B.该电池可用于闹钟、收音机、照相机等
C.该电池使用后能投入火中,也可投入池塘中
(2)目前常用的镍(Ni)镉(Cd)电池,其电池总反应可表示为: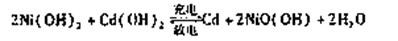
已知Ni(OH)2和Cd(OH)2均难于溶于但酸,以下说法正确的是 A.以上反应是可逆反应 B.反应环境为碱性
A.以上反应是可逆反应 B.反应环境为碱性
C.电池放电时Cd做负极 D.是一种二次电池
(3)美国阿波罗的氢氧燃料电池是一种新型电源,其构造如图所示,a、b两个电极均由多孔的碳块组成,通入氢气和氧气由孔隙中逸出,并在电极表面发生电极反应而放电。
①其电极为a是极(填正或负)
②若为飞行员提供了360kg的水,则电路中通过了mol电子。
25°C时,在体积为2L的密闭容器中,气态物质A、B、C的物质的量n(m ol)随时间t的变化如右图所示,已知达平衡后,降低温度,A的转化率将增大。
ol)随时间t的变化如右图所示,已知达平衡后,降低温度,A的转化率将增大。
(1)根据上图数据,写出该反应的化学方程式:;此反应的平衡常数表达式K=,从反应开始到达第一次平衡时的平均速率v(A)为。
(2)在5—7min内,若K值不变,则此处曲线变化的原因是
(3)下图表示此反应的反应速率v和时间t的关系图:
各阶段的平衡常数如下表所示:
 |
 |
 |
 |
 |
 |
 |
 |
K1、K2、K3、K4之间的关系为:(用“>”、“<”或“=”连接)A的转化率最大的一段时间是
已知A是乙烯,B、C、D、E均为常见的有机物,在一定条件下,它们有如下力
所示的转化关系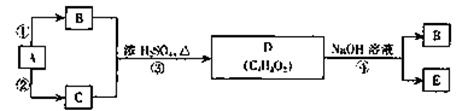
请回答:
(1)C的结构简式是
(2)能与金属钠反应放出氢气的物质有(填字母)
(3)在图示转化关系中,属于加成反应的有(填序号)
(4)A、B、C三种物质的摩尔质量由大到小的顺序是
(5)反应④的化学方程式是