已知A、B、C、D四种短周期元素在元素周期表中的相对位置如下图所示,它们的原子序数之和为46。请填空: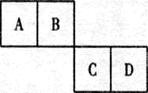
(1)B元素的名称为 D元素的原子结构示意 图为 。
(2)B有多种氧化物,其中之一是一种无色气体。该气体在空气中会迅速变成红棕色,在一定条件下,4L的该无色气体与3L的氧气相混合,被足量的水完成吸收,且只生成一种B的含氧酸,该含氧酸的化学式为 。
(3)离子半径:D﹣ C2﹣(填“>”、“<”、“=”)。还原性:D﹣ C2﹣(填“>”、“<”、“=”)。
一些常见化学反应可用下式表示 A + B → C+D+H2O其中A为单质 (必要时可加热),请你根据下面的提示回答下列问题:
(1)若A、C、D均含有氯元素,则A与B溶液反应的离子方程式为:。
(2)若C、D均为气体且有一种为红棕色,则B是。
(3)若C、D均为气体且都能使澄清石灰水变浑浊,则A与B反应的化学方程式为:。
如何稀释B的浓溶液 。
(4) 若A为紫红色的固体,D为无色无味的气体,则A与B溶液反应的离子方程式为:。若产生标准状况下4.48L的D气体,则被还原的B的物质的量是mol。
利用图所示装置收集以下4种气体(图中烧瓶的位置不得变化)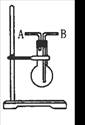
①NO ②Cl2 ③NH3 ④SO2(写序号)
(1)若烧瓶是干燥的,则由B口进气收集的气体有________;
(2)若烧瓶是干燥的,则由A口进气,可收集的气体有_______。
(3)若烧瓶充满水,可收集的气体有________,这时气体由________进入。
(4)若在烧瓶内装入浓硫酸使气体干燥,则可用此装置来干燥的气体有________,这时气体由________口进入。
工业碳酸钠(纯度约为98%)中含有Ca2+、Mg2+、Fe3+、Cl-和SO42-等杂质,提纯工艺线路如下: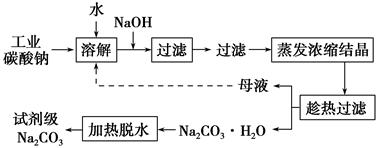
Ⅰ.碳酸钠的饱和溶液在不同温度下析出的溶质如图所示:
Ⅱ.有关物质的溶度积如下:
| 物质 |
CaCO3 |
MgCO3 |
Ca(OH)2 |
Mg(OH)2 |
Fe(OH)3 |
| Ksp |
4.96×10-9 |
6.82×10-6 |
4.68×10-6 |
5.61×10-12 |
2.64×10-39 |
回答下列问题:
(1)加入NaOH溶液时发生反应的离子方程式为:_____________________________________。
向含有Mg2+、Fe3+的溶液中滴加NaOH溶液,当两种沉淀共存且溶液的pH=8时,c(Mg2+):c(Fe3+)=________。
(2)“趁热过滤”时的温度应控制在________。
(3)有人从“绿色化学”角度设想将“母液”沿流程中虚线所示进行循环使用。请你分析实际工业生产中是否可行________,并说明理由________________________________________。
(4)已知:Na2CO3·10H2O(s)=Na2CO3(s)+10H2O(g) ΔH=+532.36 kJ·mol-1
Na2CO3·10H2O(s)=Na2CO3·H2O(s)+9H2O(g)ΔH=+473.63 kJ·mol-1
写出NaCO3·H2O脱水反应的热化学方程式________________________________________。
以黄铁矿为原料,采用接触法生产硫酸的流程可简示如下: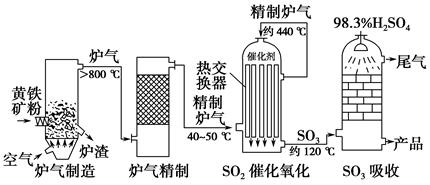
请回答下列问题:
(1)在炉气制造中,生成SO2的化学方程式为_________________________________________;
(2)炉气精制的作用是将含SO2的炉气________、________及干燥,如果炉气不经过精制,对SO2催化氧化的影响是___________________________________________;
(3)精制炉气(含SO2体积分数为7%、O2为11%、N2为82%)中SO2平衡转化率与温度及压强关系如下图所示。在实际生产中,SO2催化氧化反应的条件选择常压、450 ℃左右(对应图中A点),而没有选择SO2转化率更高的B或C点对应的反应条件,其原因分别是____________、____________;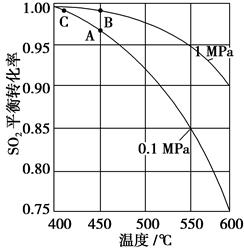
(4)在SO2催化氧化设备中设置热交换器的目的是________、________,从而充分利用能源。
工业上用粗氧化铜(含杂质FeO)为原料制取氯化铜晶体(CuCl2·2H2O)的生产流程如下: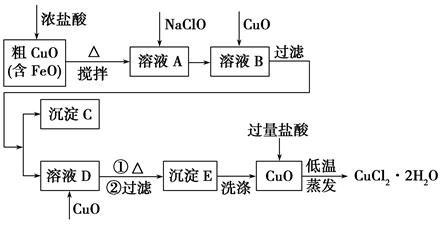
| 物质 |
Fe(OH)2 |
Cu(OH)2 |
Fe(OH)3 |
| 完全沉淀时的pH |
≥9.6 |
≥6.4 |
3~4 |
(1)写出向溶液A中加入NaClO的离子方程式___________________________________。
(2)沉淀C的化学式为________。
(3)实验室如何检验沉淀E已洗涤干净?________。
(4)低温蒸发的目的是______________________________________。
(5)流程中两次加入了CuO,而不是一次性向溶液B中加入过量的CuO,其理由是________________________________________________。