珍珠粉以其良好的养颜等功效,获得消费者喜爱。资料显示:珍珠中含碳酸钙80—93%、蛋白质4—14%、水份2—4%、十几种氨基酸、28种微量元素。然而一些不法分子用回收的贝壳加上工业用氢氧化钠配制的药水进行清洗、晾晒以后直接加工销售,其主要成分是:碳酸钙,及少量残留氢氧化钠。以下是某化学兴趣小组设计辨别真假珍珠,并测定珍珠中碳酸钙含量的实验探究方案。
【探究一】辨别市售珍珠真与假。
将其分别溶于水,充分搅拌、静置,测定上层清液的pH;若pH 7(填“>”或“<”或“=”)为假珍珠,理由是 。
【探究二】测定珍珠中碳酸钙含量。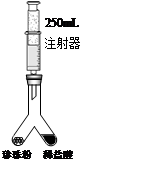
小王用图所示装置测定该珍珠粉中碳酸钙的含量。实验方案如下:
⑴检查装置气密性:按图连接装好置后,将注射器活塞(不考虑活塞的摩擦和自重,下同)从刻度1mL处向上拉至刻度20mL处, (填操作和现象),则气密性良好;
⑵在图异型装置左管内装入1.1g 上述珍珠粉样品,右管内倒入一定量的稀盐酸,注射器(规格为250mL)活塞推到底部,再次连接装置;
⑶设法使左右两管内的药品混合,反应结束后读取注射器读数为220mL;
⑷数据处理:计算得该珍珠粉中碳酸钙的质量分数为 。[ρ〔CO2〕=2g/L,结果保留小数点后1位]
【实验思考】
⑴此实验中的反应原理是 (用化学方程式表示);
⑵考虑注射器因素,该实验方案对珍珠粉的用量多少是否必须作要求? ;
⑶【探究二】中的第⑶步,混合两种药品的方法是 ;
⑷该实验装置设计上的优点在于 (写出1点即可)。
小聪同学家新换了水龙头,从说明书上了解到该水龙头是铜质镀铬。好奇的小聪想探究铬(Cr)与常见金属铁、铜的活动性强弱,邀请你一同参加。
[知识回放]
金属活动性顺序:K Ca Na Mg Al ZnSn Pb(H)Hg Ag Pt Au,请你在横线上填写对应金属的元素符号。
[作出猜想]
猜想1.Cr>Fe>Cu;猜想2.Fe>Cu>Cr;猜想3.你的猜想是。
[查阅资料]
(1)铬是银白色有光泽的金属,在空气中其表面能生成抗腐蚀的致密的氧化膜.
(2)铬能与稀硫酸反应,生成蓝色的硫酸亚铬(CrSO4)溶液.
[设计实验]
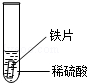
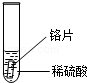
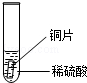
小聪同学取大小相等的三种金属片,用砂纸打磨光亮;再取三支试管,分别放入等量的同种稀硫酸
| 实验 |
试管1 |
试管2 |
试管3 |
| 实验 操作 |
 |
 |
 |
| 实验 现象 |
铁片表面产生气泡较慢,溶液变为浅绿色 |
铬片表面产生气泡较快,溶液变成为蓝色 |
[结论与解释]
(1)小聪得到的结论是猜想正确。
(2)实验前用砂纸打磨金属片的目的是。
[知识运用]
将铬片投入FeSO4溶液中,反应(填“能”或“不能”)进行.若能进行,请你写出反应的化学方程式。
某无土栽培营养液的配方中可能含有氯化钾、硫酸铵、碳酸氢氨中的一种或几种物质,为确定配方的成分,化学兴趣小组的同学开展了以下探究活动:
(1)【实验探究一】取少量固体样品在研体中与熟石灰混合研磨,有刺激性气味的气体产生,该气体能使湿润的红色石蕊试纸变色,写出可能发生该反应的一个化学方程式。
(2)【实验探究二】另取少量固体样品溶于水得到溶液A,按下图所示进行实验,现象如图所述(设发生的反应都恰好完全进行).请你回答下列问题: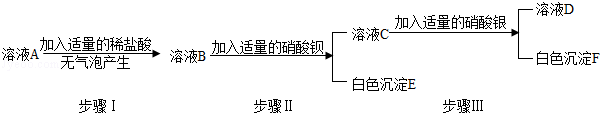
①白色沉淀E是。
②小明认为由实验探究二可以确定该化肥中一定含有氯化钾和硫酸铵,一定没有碳酸氢铵。小强认为这个结论不正确,他的理由。为了使小明的结论正确,小强对上述实验进行了改动,他的做法是。
在实验课中,各小组作了如下实验:
| 实验编号 |
1 |
2 |
3 |
4 |
| 实验操作 |
 |
 |
 |
 |
实验后,同学们按老师要求将废液都倒在指定的大烧杯中,小科猜想该烧杯中的废液可能有硫酸铜、硫酸锌、硫酸亚铁…,应该可以从中提炼出铁和铜。经思考后,他设计了如图所示的实验,并设法使滤液甲和乙所含的溶质相同。
则固体C是,操作③的名称是,实验中所加的过量金属粉末是。
对比学习有利于发现事物的共性与个性。为探究酸的性质,同学们进行了如下实验。
| 实验内容 |
实验现象 |
分析与结论 |
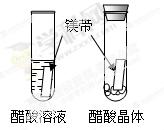 |
醋酸晶体试管内 (1),醋酸溶液试管中镁带表面冒气泡。 |
酸的很多反应通常在水溶液中才能完成。 |
用玻璃棒蘸硫酸在白纸上写字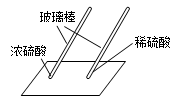 |
(2)(填“浓”或“稀”)硫酸使白纸炭化。 |
即使是同种酸,由于(3) 不同,它们的性质不完全相同。 |
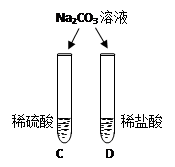 |
两试管中均产生(4) |
不同的酸具有相似的性质,这是因为酸的组成中都含有(5)(填元素符号)。 |
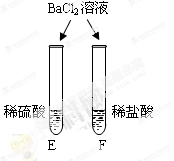 |
E试管中产生(6) , F试管中无明显现象。 |
不同的酸根会导致酸的“个性”差异。因此,可用氯化钡溶液鉴别盐酸和硫酸。 |
清洗试管时,小乔同学将C、F两试管中的无色液体同时倒入一个洁净的废液缸,废液缸中立刻冒气泡并出现白色沉淀。请分析上述现象并回答:
Ⅰ.废液缸中产生气体的化学方程式为(7) 。
Ⅱ. 废液缸里最终产生的白色沉淀中一定有硫酸钡,可能有(8) (填化学式)。
金属材料在国防建设中起着量要的作用,图1为歼﹣15飞机在辽宁舰上起飞
(1)铝合金用于制造飞机的外壳,铝合金材质的主要优点是、。
(2)改装前的辽宁舰舰身锈迹斑斑,钢铁的锈蚀主要是铁与空气中的共同作用的结果,工业生产中常用稀盐酸除去铁制品表面的铁锈,该反应的化学方程式为。
(3)为了避免轮船的钢质外壳被腐蚀,通常在轮船外壳上镶嵌比铁活动性强金属。小明为探究锌、铁、铜三种金属的活动性顺序,设计了如图2的两个实验:
①实验一中,小明以“金属表面产生气泡的快慢”为标准来判断锌、铁的活动性强弱,有同学认为不够合理,理由是。
②实验二中,若出现现象,可证明铁的活动性强于铜,该反应的化学方程式为。
(4)辽宁舰的建造耗费了大量的钢材.某兴趣小组在实验室用图3所示装置模拟炼铁的化学原理,并测定赤铁矿中氧化铁的质量分数(装置气密性良好,反应完全且赤铁矿中的杂质不参加反应,称量赤铁矿样品的质量为wg)。
①装置A中生成铁的化学方程式为,装置B中发生反应的化学方程式为。
②要测定该赤铁矿样品中氧化铁的质量分数,需要测量的数据是。