T ℃时,在2 L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如右图所示,下列描述正确的是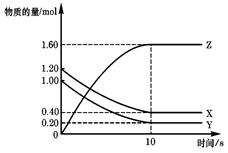
| A.平衡时X、Y的转化率相同 |
| B.达到平衡后,将容器体积扩大为4 L,平衡逆向移动 |
| C.平衡时X的正反应速率与Y的逆反应速率相等 |
D.T℃时,该反应的化学方程式为:X (g)+Y(g)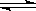 2Z(g),平衡常数K="40" 2Z(g),平衡常数K="40" |
室温下,有下列四种溶液:①0.1mol·L-1氨水,
②0.1mol·L-1 NH4Cl溶液,③0.2mol·L-1盐酸与0.2mol·L-1NH4Cl
溶液等体积混合,④0.2mol·L-1NaOH溶液与0.2mol·L-1氨水等体
积混合,四种溶液中c(NH )由大到小排列正确的是()
)由大到小排列正确的是()
| A.②③④① | B.④①②③ | C.①④②③ | D.③②①④ |
在25℃浓度均为1mo l · L-1的(NH4)2SO4, (NH4)2Fe(SO4)2,(NH4)2CO3溶液中,测得c(NH4+)分别为a,b,c (单位mo l · L-1)则下列关系式正确的是( ).
A a=b=c
B a>b>c
C a>c>b
D b>a>c
在0.1mol·L-1的Na2CO3溶液中下列关系式正确的是( ).
A c(OH-)=c(H+)+c(HCO3-)+2c(H2CO3)
B c(OH-)=c(H+)+c(HCO3-)
C c(OH-)=c(H+)+2c(H2CO3)
D c(OH-)=c(H+)+c(HCO3-)+c(H2CO3)
35℃时,在0.1mol·L-1的Na2S,NaHS两溶液中均存在的关系是( ).
A c(OH-)×c(H+)=1×10-14
B c(Na+)=c(S2-)+c(HS-)+c(H2S)
C c(OH-)=c(H+)+c(HS-)+2c(H2S)
D c(Na+)+c(H+)=c(OH-)+c(HS-)+2c(S2-)
向3mo l · L-1的NaOH溶液100mL中缓缓地通入4.48L(标准状况)二氧化碳气体,充分反应后,溶液中离子浓度由大到小排列顺序正确的是()。
A c(Na+) > c(CO32-) > c(HCO3-) > c(OH-) > c(H+)
B c(Na+) > c(CO32-) = c(HCO3-) > c(OH-) > c(H+)
C c(Na+) > c(HCO3-) >c(OH-) > c(CO32-) > c(H+)
D c(Na+) > c(HCO3-) > c(CO32-) >c(OH-) > c(H+)