高温下,炽热的铁与水蒸气在一个体积可变的密闭容器中进行反应:
3Fe(s)+4H2O(g)=Fe3O4(s)+4H2(g),下列条件的改变对其反应速率几乎无影响的是( )
| A.把铁块变成铁粉 | B.将容器的体积缩小一半 |
| C.压强不变,充入氮气使容器体积增大 | D.体积不变,充入氮气使容器压强增大 |
A、B、C、X均为中学常见的物质,它们之间有如下转化关系(其它产物已略去):
则下列说法不正确的是
A.若A是NH3,则C可能是氧化物
B.若A是非金属单质,则C与水反应的生成物一定是强酸
C.若X是金属单质,则B、C中X的化合价可能是B>C
D.若X是强碱,则B可能是两性物质
实验室将9 g铝粉跟一定量的金属氧化物粉末混合形成铝热剂。发生铝热反应之后,所得固体中含金属单质为18g,则该氧化物粉末可能是
g铝粉跟一定量的金属氧化物粉末混合形成铝热剂。发生铝热反应之后,所得固体中含金属单质为18g,则该氧化物粉末可能是
A.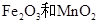 B.
B.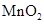 和
和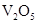
C.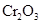 和
和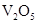 D
D 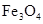 和FeO
和FeO
氧化还原反应中,水的作用可以是氧化剂、还原剂、既是氧化剂又是还原剂、既非氧化剂又非还原剂等。下列反应与Br2+SO2+2H2O=H2SO4+2HBr相比较,水的作用不相同的是
| A.2Na2O2+2H2O=4NaOH+O2↑ | B.4Fe(OH)2+O2+2H2O=4Fe(OH)3 |
| C.2F2+2H2O=4HF+O2 | D.2Al+2NaOH+2H2O=2NaAlO2+3H2↑ |
要配制浓度约为2 mol·L-1 NaOH溶液100mL,下面的操作正确的是
| A.称取8 g NaOH固体,放入250 mL烧杯中,用100 mL量筒量取100 mL蒸馏水,加入烧杯中,同时不断搅拌至固体溶解 |
| B.称取8 g NaOH固体,放入100 mL量筒中,边搅拌,边慢慢加入蒸馏水,待固体完全溶解后用蒸馏水稀释至100 mL |
| C.称取8 g NaOH固体,放入100 mL容量瓶中,加入适量蒸馏水,振荡容量瓶使固体溶解,再加入水到刻度,盖好瓶塞,反复摇匀 |
| D.用100 mL量筒量取40 mL 5 mol·L-1NaOH溶液,倒入250 mL烧杯中,再用同一量筒取60 mL蒸馏水,不断搅拌下,慢慢倒入烧杯中 |
下列实验方案中,可以测定Na2CO3和NaHCO3混合物中Na2CO3质量分数的是
①取a克混合物与足量稀盐酸充分反应,取产生的气体体积bmL(折算为标况)
②取a克混合物与足量稀盐酸充分反应,加热、蒸干、灼烧,得b克固体
③取a克混合物充分加热,减重b克
| A.只有①② | B.只有②③ | C.只有③ | D.全部可以 |