下图表示从固体混合物中分离X的两种方案,请回答有关问题。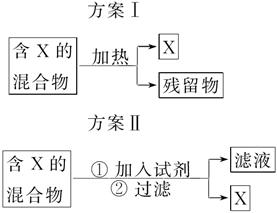
(1)选用方案Ⅰ时,X应该具有的性质是____________,残留物应该具有的性质是__________________;
(2)选用方案Ⅱ从某金属粉末(含有Au、Ag和Cu)中分离Au,加入的试剂是________,有关反应的化学方程式为
________________________________________________________________________;
(3)为提纯某Fe2O3样品(主要杂质有SiO2、Al2O3),参照方案Ⅰ和Ⅱ,请设计一种以框图形式表示的实验方案(注明物质和操作)。
研究物质的结构是研究物质性质的的基础,分析下列微粒的结构,完成问题:
(1) 根据VSEPR理论,BCl3的立体结构为:_______________,HCN的立体结构为:_________________。(文字表述,不必画图)两分子中中心原子的杂化类型分别为_________ ___________ 。
(2)原子序数小于36的元素Q和T,在周期表中既处于同一周期又位于同一族,且原子序数T比Q多2。T的基态原子外围电子(价电子)排布式为 ,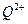 的未成对电子数是。
的未成对电子数是。
(3) 中的
中的 与
与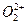 互为等电子体。已知
互为等电子体。已知 、
、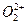 两种粒子中各原子最外层均为8电子稳定结构。
两种粒子中各原子最外层均为8电子稳定结构。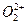 的电子式可表示为 ;
的电子式可表示为 ;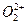 中含有的
中含有的 键数目为。
键数目为。
(1)试写出短周期元素形成的含有14个电子的分子(至少三种)的化学式:,其中和互为等电子体。
(2)CH3CHO分子中,-CH3中的碳原子采用杂化方式,-CHO中的碳原子采取杂化方式。
 Q、R、X、Y、Z五种元素的原子序数依次递增。已知:
Q、R、X、Y、Z五种元素的原子序数依次递增。已知: ①Z的原子序数为29,其余的均为短周期主族元素;
①Z的原子序数为29,其余的均为短周期主族元素; ②Y原子价电子(外围电子)排布msnmpn;
②Y原子价电子(外围电子)排布msnmpn; ③R原子核外L层电子数为奇数;
③R原子核外L层电子数为奇数; ④Q、X原子p轨道的电子总数分别为2和4。
④Q、X原子p轨道的电子总数分别为2和4。 请回答
请回答 下列问题:
下列问题: (1)Z2+ 的核外电子排布式是。
(1)Z2+ 的核外电子排布式是。 (2)在[Z(NH3)4]2+离子中,Z2+的空间轨道受NH3分子提供的形成配位键。
(2)在[Z(NH3)4]2+离子中,Z2+的空间轨道受NH3分子提供的形成配位键。 (3)Q与Y形成的最简单气态氢化物分别为甲、乙,下列判断正确的是。
(3)Q与Y形成的最简单气态氢化物分别为甲、乙,下列判断正确的是。 a.稳定性:甲>乙,沸点:甲>乙 b.稳定性:甲>乙,沸点:甲<乙
a.稳定性:甲>乙,沸点:甲>乙 b.稳定性:甲>乙,沸点:甲<乙 c.稳定性:甲<乙,沸点:甲<乙 d.稳定性:甲<乙,沸点:甲>乙
c.稳定性:甲<乙,沸点:甲<乙 d.稳定性:甲<乙,沸点:甲>乙 (4) Q、R、Y三种元素的第一电离能数值由小到大的顺序为(用元素符号作答)
(4) Q、R、Y三种元素的第一电离能数值由小到大的顺序为(用元素符号作答) (5)Q的一种氢化物分子中质子总数为14,其中分子中的σ键与π键的键数之比为。
(5)Q的一种氢化物分子中质子总数为14,其中分子中的σ键与π键的键数之比为。

 已知X、Y和Z三种元素的原子序数之和等于42。X元素原子的4p轨道上有3个未成对电子,Y元素原子的最外层2p轨道上有2个未成对电子,其余电子均成对。X跟Y可形成化合物X2Y3,Z元素可以形成负一价离子。请回答下列问题:
已知X、Y和Z三种元素的原子序数之和等于42。X元素原子的4p轨道上有3个未成对电子,Y元素原子的最外层2p轨道上有2个未成对电子,其余电子均成对。X跟Y可形成化合物X2Y3,Z元素可以形成负一价离子。请回答下列问题: (1)X元素在元素周期表中的位置为__________,该元素的符号是__________;
(1)X元素在元素周期表中的位置为__________,该元素的符号是__________; (2)Y元素原子的价层电子的轨道表示式(即价电子排布图)为_____ ,该元素的名称是__________。
(2)Y元素原子的价层电子的轨道表示式(即价电子排布图)为_____ ,该元素的名称是__________。 (3)X
(3)X 与Z可形成化合物XZ3,该化合物分子为含________键的________分子(填“极性” 或“非极性”)。
与Z可形成化合物XZ3,该化合物分子为含________键的________分子(填“极性” 或“非极性”)。 (4)
(4) 比较X的氢化物与同族第二、第三周期元素所形成的氢化物稳定性、沸点高低并说明沸点高低的理由。(用化学式表示)
比较X的氢化物与同族第二、第三周期元素所形成的氢化物稳定性、沸点高低并说明沸点高低的理由。(用化学式表示)
稳定性由强到弱的顺序为____________。沸点由高到低的顺序为______________,
理由是____________。
(8 分)
分)
X、Y、Z、W是元素周期表前四周期中的四种常见元素,其相关信息如下表:
| 元素 |
相关信息 |
| X |
X的基态原子核外3个能级上有电子,且每个能级上的电子数相等 |
| Y |
常温常压 下,Y单质是淡黄色固体,常在火山口附近沉积 下,Y单质是淡黄色固体,常在火山口附近沉积 |
| Z |
Z和Y同周期,Z的电负性大于Y |
| W |
W的一种核素的质量数为63,中子数为34 |
(1)X原子共有种不同运动状态的电子。Y和Z的最高价氧化物对应的水化物的酸性较强的是 (写化学式)。
(2)XY2是一种常用的溶剂,XY2的分子中存在 个σ键。
在H―Y、H―Z两种共价键中,键的极性比较:H―Y H―Z,键长H―Y H―Z。(填>或<)
(3)W的基态原子外围电子排布式是 。W2Y在空气中煅烧生成W2O的化学方程式是 。