电解原理在化学工业中有广泛的应用。如下图表示一个电解池,装有电解液c;A、B分别是两块电极板,通过导线与直流电源相连。
(1)若A、B都是惰性电极,电解质溶液c是饱和NaCl溶液,实验开始时,同时在U形管两边各滴入几滴酚酞试液,试判断:
①a是________极(填“正”或“负”),B是________极(填“阴”或“阳”);
②A电极上的电极反应式为
________________________________________________________________________,
B电极上的电极反应式为
________________________________________________________________________;
③检验A电极产物的方法是
________________________________________________________________________
________________________________________________________________________。
(2)如用电解法精炼粗铜,电解液c选用CuSO4溶液,则
①A电极的材料是________,电极反应式为
________________________________________________________________________
______________;
②B电极的材料是________,电极反应式为
________________________________________________________________________
______________。
(3)用惰性电极电解CuSO4溶液。若阴极上析出Cu的质量为3.2 g,则阳极上产生的气体在标准状况下的体积为________;常温下,若将电解后的溶液稀释至1 L,则溶液的pH约为________。
比较法是化学中研究物质性质的基本方法之一,请运用比较法解答下题。Na2O2几乎可与所有的常见气态非金属氧化物反应。如2Na2O2+2CO2 ="=" 2Na2CO3+O2,Na2O2+CO= Na2CO3。
(1)通过比较可知,当非金属元素处于____________价时,其氧化物与Na2O2反应有O2生成。
(2)试分别写出Na2O2与SO2、SO3反应的化学方程式:_____________;_____________。
(3)氰(CN)2的化学性质和卤素(X2)很相似,化学上称为拟卤素。试写出(CN)2与水反应的化学方程式:______________________________。
根据反应8NH3+3Cl2=6NH4Cl+N2,回答下列问题:
(1)该反应中氧化剂是 ,被氧化的是 元素。
(2)用双线桥法标出电子转移的方向与数目。
(3)该反应中参加氧化还原的氧化剂与还原剂的物质的量之比为 。
碘被称为“智力元素”,科学合理地补充碘可防止碘缺乏病,KI、KIO3曾先后用于加碘盐中。
(1)工业上可以通过铁屑法生产KI,其工艺流程如下:
①反应I生成铁与碘的化合物(Fe3I8),若该化合物中铁元素与碘元素的质量比_______,则反应Ⅱ的化学方程式是________________________________。
②操作A包括加热浓缩、______________、______________;用冰水洗涤的目的是______________。
(2)KIO3可以通过H2O2氧化I2先制得HIO3,然后再用KOH中和的方法进行生产。
①配平第一步反应的化学方程式:___H2O2+___I2→____HIO3+____H2O
②烹饪时,含KIO3的食盐常在出锅前加入,其原因是_______________________。
③若制得1.284 kg KIO3固体,理论上至少需消耗质量分数为30%的双氧水__________kg。
喷泉实验是一种常见的自然现象,其产生原因是存在压强差。试根据下图,回答下列问题:
(1)在图A的烧瓶中充满干燥气体,胶头滴管及烧杯中分
别盛有液体。下列组合中不可能形成喷泉的是()。
A.HCl和H2O B.Cl2和NaOH溶液
C.HCl和汽油 D.CO2和NaOH溶液
(2)在图B的锥形瓶中,分别加入足量的下列物质,反应后可能产生喷泉的是()
A.Cu与稀盐酸 B.NaHCO3与NaOH溶液
C.CaCO3与稀硫酸 D.NH4HCO3与稀盐酸
(3)在图B的锥形瓶外放一水槽,锥形瓶中加入酒精,水槽中加入冷水后,再加入足量的下列物质,结果也产生了喷泉。水槽中加入的物质不可能是()
A.浓硫酸 B.生石灰 C.硝酸铵 D.烧碱
实验室制备气体时,可根据反应物的状态、反应条件和生成气体的性质来选择气体的发生装置。
| 编号 |
A |
B |
C |
发 生 装 置 |
 |
 |
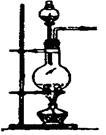 |
(1)实验室用氯酸钾和二氧化锰制氧气时,可选用的发生装置是 (写编号);
(2)实验室用食盐固体和浓硫酸制氯化氢气体时,可选用的发生装置是 (写编号),写出微热时的反应方程式 ;
(3)高锰酸钾和二氧化锰都是强氧化剂,均可将浓盐酸氧化为氯气。
(a) 用浓盐酸和高锰酸钾制氯气的反应方程式如下:
2KMnO4 + 16HCl 2KCl + 2MnCl2 + 5Cl2 ↑ + 8H2O
2KCl + 2MnCl2 + 5Cl2 ↑ + 8H2O
①用“单线桥”在上述方程式上标出电子转移的方向和数目。
②反应中 元素被氧化, 是氧化剂。当有1mol电子转移时,可生成气体 升(标准状态下)。
(b) 用浓盐酸和二氧化锰制氯气的实验装置如图所示: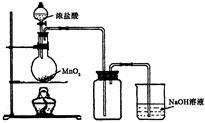
写出圆底烧瓶中发生反应的化学方程式_
②实验结束清洗仪器时,为了减少烧瓶中残留氯气对环境的污染,可以向烧瓶中加入的溶液是________,有关的化学方程式_________________________.