从H+、K+、Cu2+、Cl-、SO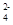 中选取适当的离子组成符合下列情况的电解质,进行电解(阳离子只能使用一次)。
中选取适当的离子组成符合下列情况的电解质,进行电解(阳离子只能使用一次)。
(1)以碳棒为电极进行电解,电解质的物质的量减少,水的物质的量保持不变,两极都有气体生成,气体体积相同,则该电解质的化学式为____________,电解的阴极反应____________,电解的阳极反应________________________,电解的总方程式是______________________。
(2)以铂丝为电极进行电解,水的物质的量减少,电解质的物质的量保持不变,两极都有气体生成,气体体积比为2:1,则该电解质的化学式为____________________,阴极反应式为____________________,阳极反应式为___________________________。
(3)惰性电解,电解质的物质的量减少,水的物质的量也减少,pH下降,则电解质的化学式为____________,电解的总方程式为__________________________________。
某结晶水合物含有两种阳离子和一种阴离子。称取两份质量均为 45.3g 的该结晶水合物,分别制成溶液。向其中一份逐滴加人 NaOH 溶液,开始发现溶液中出现白色沉淀并逐渐增多;一段时间后有气体逸出,该气体有刺激性气味,能使湿润的红色石蕊试纸变蓝,加热后共计可收集到 2.24L 该气体(标准状况);最后白色沉淀逐渐减少并最终消失。另一份逐滴加人 Ba (OH)2溶液,开始现象类似,但最终仍有白色沉淀;过滤,用稀硝酸处理沉淀物,经洗涤和干燥,得到白色固体 46.6g 。
请回答以下问题:
(1)该结晶水合物中含有的两种阳离子是______和_________,阴离子是___________。
(2)试通过计算确定该结晶水合物的化学式。
(3)假设过程中向该溶液中加人的 NaOH 溶液的物质的量浓度为5mol·L一1,请在右图中画出生成沉淀的物质的量与加入 NaOH 溶液体积的关系示意图。
某学生利用氯酸钾分解制氧气的反应,测定氧气的摩尔质量。实验步骤如下:
①装好实验装置。②检查装置气密性。③把适量的氯酸钾粉末和少量二氧化锰粉末混合均匀,放入干燥的试管中,准确称量,质量为ag。
④加热,开始反应,直到产生一定量的气体。
⑤停止加热(如图,导管出口高于液面)。
⑥测量收集到气体的体积。
⑦准确称量试管和残留物的质量为bg。
⑧测量实验室的温度。
⑨把残留物倒入指定的容器中,洗净仪器,放回原处,把实验桌面收拾干净。
⑩处理实验数据,求出氧气的摩尔质量。
回答下列问题:
(1)如何检查装置的气密性?
(2)以下是测量收集到气体体积必须包括的几个步骤;①调整量简内外液面高度使之相同;②使试管和量筒内的气体都冷却至室温;③读取量筒内气体的体积。这三步操作的正确顺序是:(请填写步骤代号)。
(3)测量收集到气体体积时,如何使量筒内外液面的高度相同?。
(4)如果实验中得到的氧气体积是c L(已换算成标准状况下),水蒸气的影响忽略不计,氧气的摩尔质量的计算式为(含a、b、c,不必化简):M(O2)=。
已知氨气跟氯气可迅速反应生成氯化铵和氮气。当转移的电子总数为a个时,生成的氮气的物质的量bmol.
 (1)写出该反应配平的化学方程式:
(1)写出该反应配平的化学方程式: (2)该反应中参加氧化还原反应的氧化剂和还原剂的物质的量之比为。
(2)该反应中参加氧化还原反应的氧化剂和还原剂的物质的量之比为。 (3)阿伏加德罗数常数为(用含a、b的代数式表示)。
(3)阿伏加德罗数常数为(用含a、b的代数式表示)。
取等物质量浓度的NaOH溶液两份,每份为50ml。向其中通入一定量的CO2,随后分别取溶液10ml,将其稀释成100ml,并分别向稀释后的溶液中逐滴加入0.1mol/L的HCI溶液,产CO2的体积(标准状况)与加入盐酸体积之间的关系如图所示(设分别为A、B两种情况)。
 回答下列问题:
回答下列问题: (1)在(A)情况下,溶质为(写化学式),其物质的量之比为,在标准状况下,通人CO2气体的体积为 。
(1)在(A)情况下,溶质为(写化学式),其物质的量之比为,在标准状况下,通人CO2气体的体积为 。 (2)在(B)情况下,溶质为(写化学式),其物质的量之比为,在标准状况下,通人CO2气体的体积为 。
(2)在(B)情况下,溶质为(写化学式),其物质的量之比为,在标准状况下,通人CO2气体的体积为 。 (3)原NaOH溶液的物质的量浓度为 。
(3)原NaOH溶液的物质的量浓度为 。
一定量的氢气在氯气中燃烧,所得混合物用100
3.00
溶液(密度为1.12
)恰好完全吸收,测得溶液中含有
的物质的量为0.0500
。
(1)原
溶液的质量分数为。
(2)所得溶液中
的物质的量为
。
(3)所用氯气和参加反应的氢气的物质的量之比
=。