某种ABS工程树脂,由丙烯腈(CH2=CHCN,符号A),1,3—丁二烯(CH2=CHCH=CH2,符号B)和苯乙烯( —CH=CH2,符号S)按一定配比共聚而得。
—CH=CH2,符号S)按一定配比共聚而得。
(1) A,B和S三种单体中,碳氢比(C:H)值最小的单体是____________________
(2) 经元素分析可知该ABS样品的组成为CaHbNc(a,b,c为正整数),则原料中A和B的物质的量之比是________________(用a,b,c表示)。
(1)氟里昂是freon的音译名,氟里昂的商业代号可用HFC—nmp表示,其中数字n等于碳原子数目减1(如果是0就省略),数字m等于氢原子数目加1,数字p等于氟原子数,氯原子数目不列。则氟里昂CH2F-CHF2的代号为,它属于(填“一卤代烃”“多卤代烃”“不饱和卤代烃”“芳香卤代烃”)类有机物,其同分异构体的结构简为;
⑵由于氟里昂无毒,化学性质又极其稳定,被大量用于制冷剂、灭火剂、发泡剂等。但大气中的氟里昂在平流层中受紫外线照射,会分解产生Cl原子,而Cl原子化学性质比较活泼: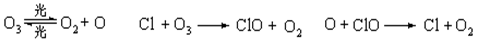
上述反应的总反应为,反应过程中,Cl原子起作用;
⑶O3和O2的关系是;
A.同分异构体 B.同系物 C.氧的同素异形体 D.氧的同位素
⑷近几年市面上推出的冰箱新产品---无氟冰箱,主要是为了。
A.氟里昂价格高,为了经济 B.保护生态环境
C.保护人类生存环境 D.吸收和阻挡紫外线
家用不粘锅的表面涂有一层物质,它是聚四氟乙烯,请写出合成此聚合物的单体是。
抗酸药主要用于治疗____________的疾病。用离子方程式表示“胃舒平” (主要成份是氢氧化铝)治疗胃酸过多的原理_____________________________
下表是某地区市场上销售的一种“加碘食盐”包装袋上的部分文字说明。请根据此表,结合化学知识,回答下列问题。
| 配料表 |
精制海盐、碘酸钾 |
| 含碘量 |
20~40mg/kg |
| 卫生许可证号 |
××卫碘字(1999)第001号 |
| 分装日期 |
见封底 |
| 储藏方法 |
密封、避光、防潮 |
| 食用方法 |
烹调时,待食品熟后加入碘盐 |
(1)该“加碘食盐”的主要成分是(填化学式)
(2)食盐中加碘,这碘指的是(填物质名称或化学式),其中碘元素的化合价为__________价。
(3)加碘盐的食用方法中说明,烹调时,待食品熟后加入碘盐的原因是______________
我国规定饮用水质量标准必须符合下列要求
| pH |
6.5~8.5 |
| Ca2+、Mg2+总浓度 |
<0.0045mol·L-1 |
| 细菌总数 |
<100个/mL |
以下是源水处理成自来水的工艺流程示意图:源水 曝气池
曝气池 一级沉降池
一级沉降池 二级沉降池
二级沉降池 过滤池
过滤池 自来水
自来水
(1)FeSO4·7H2O是常用的凝聚剂,它在水中最终生成__________
(2)气体A的作用是。这种作用是基于(气体A和水反应的产物具有__________性。
(3)下列物质中可以作为气体A的代用品_________(填写编号)。
①Ca(ClO)2②NH3(液)③K2FeO4④SO2