纳米TiO2在涂料、光催化、化妆品等领域有着极其广泛的应用,制备纳米TiO2的方法之一是TiCl4水解生成TiO2·xH2O,经过滤、水洗除去其中的Cl-,再烘干、焙烧除去水分得到粉体TiO2。
用现代分析仪器测定TiO2粒子的大小。用氧化还原滴定法测定TiO2的质量分数:一定条件下,将TiO2溶解并还原为Ti3+,再以KSCN溶液作指示剂,用NH4Fe(SO4)2标准溶液滴定Ti3+至全部生成Ti4+。
请回答下列问题:
(1)TiCl4水解生成TiO2·xH2O的化学方程式为
________________________________________________________________________
________________________________________________________________________。
(2)检验TiO2·xH2O中Cl-是否被除净的方法是
________________________________________________________________________
________________________________________________________________________。
(3)下列可用于测定TiO2粒子大小的方法是________(填字母代号)。
a.核磁共振法 b.红外光谱法
c.质谱法 d.透射电子显微镜法
(4)配制NH4Fe(SO4)2标准溶液时,加入一定量H2SO4的原因是______________________;
使用的仪器除天平、药匙、玻璃棒、烧杯、量筒外,还需要下图中的________(填字母代号)。
(5)滴定终点的现象是
________________________________________________________________________。
(6)滴定分析时,称取TiO2(摩尔质量为M g·mol-1)试样W g,消耗c mol·L-1NH4Fe(SO4)2标准溶液V mL,则TiO2质量分数表达式为________。
(7)判断下列操作对TiO2质量分数测定结果的影响(填“偏高”、“偏低”或“无影响”)
①若在配制标准溶液过程中,烧杯中的NH4Fe(SO4)2溶液有少量溅出,使测定结果________。
②若在滴定终点读取滴定管刻度时,俯视标准液液面,使测定结果________。
小苏打(NaHCO3)试样中含有碳酸钠晶体(Na2CO3·10H2O),为测定试样中小苏打的质量分数ω(NaHCO3),实验小组同学设计了如下装置进行实验。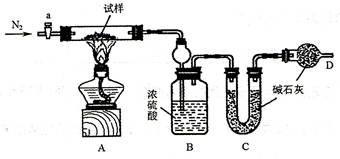
[实验过程]
①按图组装仪器,检查装置的气密性;
②将m1g试样放入硬质玻璃管中,装置B、C、D 中药品如图,己知加药品后装置B的质量为m2 g装置C 的质量为m3g;
③关闭活塞a,点燃酒精灯加热试样,直到B 装置中无气泡冒出后,打开活塞a 向装置中通人N2,一段时间后,撤掉酒精灯,关闭活塞a;
④称得装置B 的质量为m4g、装置C 的质量为m5g。
请回答以下问题(装置中原有空气对实验的影响忽略不计):
⑴装置A中发生反应的化学方程式为____________________________________
⑵装置B的作用为__________________________________________
装置C的作用为________________________________________________
⑶实验过程中通入N2的目的为__________________________________________
⑷用下列各项所提供的数据能计算出ω(NaHCO3)的是____________(填选项字母)。
| 序号 |
a |
b |
c |
d |
e |
| 数据 |
m1、m2、m3 |
m2、m3、 m4、m5 |
m1、m2、m4 |
m1、m4、m5 |
m1、m3、m5 |
⑸实验结束后发现装置A 中硬质玻璃管右端有水珠,你认为利用实验中所提供的数据还能否得到准确的ω(NaHCO3),若能,则ω(NaHCO3)的计算式为:__________________;若不能,此问不作答。
(14分) 某化学兴趣小组欲验证:“铜和一定量的浓硝酸反应有一氧化氮产生”。设计使用了如下装置进行实验。(假设气体体积均为标准状况,导气管中气体体积忽略不计,且忽略反应中的溶液体积变化)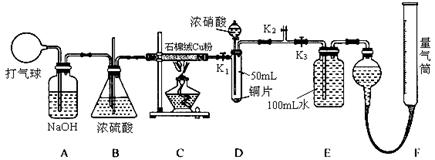
试回答下列问题:
(1)将铜粉分散在石棉绒中的原因是___________________________________。
(2)在铜和浓硝酸反应前,挤压打气球,经A、B、C反应后,进入D中的气体主要成分是_________(填化学式),通入该气体的目的是_________________________________;进行此步操作时应关闭_________,打开_________ (填K1、K2或K3)。
(3)关闭K1、K2,打开K3,由分液漏斗向D中滴加浓硝酸。待Cu和浓硝酸反应结束后,再通过分液漏斗向D中加入CCl4至满。则D中一定发生反应的离子方程式为:_______________________________________________________________________。
(4)若E中出现倒吸,可采取的应急操作是_________________________________。
(5)Ⅰ.从E装置所得溶液中取出25.00mL,加两滴酚酞,用0.1000 mol·L-1的NaOH溶液滴定,当滴定完成后消耗NaOH溶液18.00mL,则E容器中所得硝酸的物质的量浓度为__________________ mol·L-1。
Ⅱ.若实验测得F装置所收集到的气体体积为139.00 mL,则铜和一定量的浓硝酸反应___________(填“有”或“无”)NO生成,其依据是(请用数据和文字说明)__________________________________________________________________________________________________________________________________________________________________________________________________________________________。
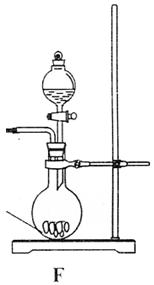
为了测定乙醇的分子结构,有人设计了图甲所示的用无水乙醇与钠反应并测定H2的体积的实验装置。回答下列有关问题:
(1)乙醇与钠反应方程式为:__________________________________________________。
(2)按图将仪器装配好,降低C管,使B、C两管间出现15~20cm水位差异后停止。该操作的目的是。
(3)已知无水乙醇密度为0.789g/mL,现取0.5mL无水乙醇,将0.25mL无水乙醇慢慢推入A中,使之与钠充分反应,则A中至少应加入钠的质量为。(小数点后保留一位数字)
(4)注射器中吸入0.5mL无水乙醇,将称好的钠放入A中,在将乙醇推入A中之前应该进行的操作是。
(5)也有人设计了如图乙所示的测定乙醇的分子结构的装置。试分析实验装置甲与实验装置乙相比,优点有(填出两点即可)。
某研究性学习小组拟通过铜银合金与浓硝酸的反应,测定该合金的组成。考虑到NO2的聚合,该小组同学查阅到下列资料:
17℃、1.01×105Pa,2NO2(g) N2O4(g) 的平衡常数K=13.3,该条件下密闭容器中N2O4和NO2的混合气体达到平衡时c(NO2)="0.0300" mol·L-1。
N2O4(g) 的平衡常数K=13.3,该条件下密闭容器中N2O4和NO2的混合气体达到平衡时c(NO2)="0.0300" mol·L-1。
⑴此时平衡混合气体中c(N2O4)=(保留两位有效数字,下同)。
⑵17℃、1.01×105Pa时,将12.44g合金放入足量浓硝酸中,待合金完全溶解后,收集到NO2和N2O4的混合气体5.00L。
①根据平衡体系中NO2和N2O4的物质的量浓度,计算5.00L气体中NO2、N2O4的物质的量分别为、。
②计算合金中银的质量分数。
(1)某化学兴趣小组的同学进行Cl2、NH3的制备、性质等实验的流程和部分装置如下:

①请利用A、G装置设计一个简单的实验验证Cl2、Fe3+、I2 的氧化性强弱为Cl2>Fe3+>I2(实验中不断小心振荡G装置中的试管)。请回答A中发生反应的离子方程式 ,试剂M为 溶液,证明氧化性为Cl2>Fe3+>I2的实验现象是 ;
②已知3Cl2 +2 NH3 =" 6HCl" + N2 ,当D的烧瓶中充满黄绿色气体后,关闭a、c打开b ,D中的现象为 ,反应一段时间后,关闭b打开c,观察到的现象为 ;
③为使实验顺利进行,请简述F中的分液漏斗的正确操作方法 ;
(2)某废水中含有一定量的Na+、SO32-,可能含有CO32-,某研究小组欲测定其中SO32-离子的浓度,设计如下实验方案:
①从下列试剂中选择试剂x为 (填序号):
A.0.1 mol·L-1 KMnO4(H2SO4酸化)溶液 B.0.5 mol·L-1 1NaOH溶液
C.新制氯水 D.KI溶液
②加入试剂x生成SO42-的离子方程式为 ;
③第ⅲ步的“系列操作”包含的操作名称为 、 、 ;
④证明该废水中是否含有CO32-的实验方案为 。