下列结构简式中,Ⅰ是扑热息痛,Ⅱ是阿司匹林,它们都是临床应用广泛的解热镇痛药,但Ⅰ易导致肾脏毒性,Ⅱ对胃黏膜有刺激性,多用会引起胃溃疡。Ⅲ是扑炎痛,它是根据药的合成中称为“拼合原理”的手段设计并合成出的解热镇痛药。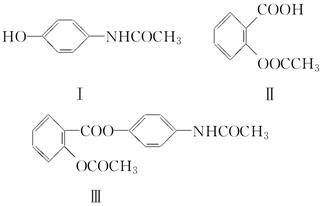
(1)为什么阿司匹林会有上述的副作用?
________________________________________________________________________。
(2)合成扑炎痛反应的反应类型为
________________________________________________________________________。
(3)扑炎痛本身并无解热镇痛效能,但口服后人体内会产生上述药理作用,且毒副作用没有Ⅰ和Ⅱ那么明显,其原因是
________________________________________________________________________
________________________________________________________________________。
物质A是由A元素组成的单质,将其在酒精灯火焰上灼烧, 火焰为黄色,B,C,D是含有A元素的三种不同化合物,A、B、C、D按右图关系进行转化: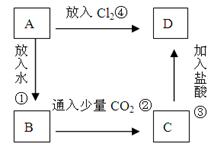
⑴写出化学式:BC
⑵写出①②反应的化学方程式。
①
②
学习化学应该明确“从生活中来,到生活中去”道理。在生产生活中,我们会遇到各种各样的化学反应。
(1) 明矾[KAl(SO4)2]是一种盐。其在水中的电离方程式是 ,明矾的用途是 。
(2)微粒32X2- 核外有18个电子,则它的核电荷数为 ,核内中子数为 。
(3)工业上用铝粉还原一些金属氧化物,这类反应称为铝热反应。写出在高温下铝还原氧化铁的化学方程式_______________________________________,在反应中消耗2mol铝,则转移了_________mol电子
(4)用氢氧化铝治疗胃酸过多的离子方程式:
(5)工业生产漂白粉的化学方程式
在Al2O3、CO2、MgO、Na2CO3、NaHCO3、Cl2物质中
⑴大气中过多会造成温室效应的是_______________.
⑵俗名是小苏打,且是制糕点发酵粉的主要成分的是________
⑶熔点高达2800℃,常用作耐高温材料的是__________________
⑷是铝土矿的主要成分_______________
⑸能用于制造漂白粉的是__________________
⑹俗名是纯碱,工业上用于造纸业的是__________
在一容积为2 L的密闭容器中,加入0.2 mol的N2和0.6 mol的H2,在一定条件下发生反应:N2(g)+3H2(g) 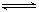 2NH3(g) ΔH<0 。反应中NH3的物质的量浓度的变化情况如下图所示,请回答下列问题:
2NH3(g) ΔH<0 。反应中NH3的物质的量浓度的变化情况如下图所示,请回答下列问题: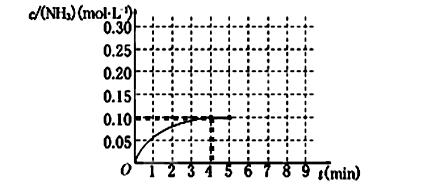
(1)根据上图,计算从反应开始到平衡时,氢气的平均反应速率v(H2)为______________。
(2)该反应达到平衡时N2的转化率_________________。
(3)反应达到平衡后,第5分钟末,保持其它条件不变,若改变反应温度,则NH3的物质的量浓度不可能为____________。(填序号)
a.0.20 mol·L-1 b.0.12 mol·L-1 c.0.10 mol·L-1 d.0.08 mol·L-1
(4)请写出该反应的平衡常数表达式_________,若该反应在298K、398K时的化学平衡常数分别为K1、K2,则K1K2(填“>”、“="”" 或 “<” )。
(5)在第5分钟末将容器的体积缩小一半后,若在第8分钟末达到新的平衡(此时NH3的浓度约为0.25 mol·L-1),请在上图中画出第5分钟末到此平衡时NH3浓度的变化曲线。
某兴趣小组同学利用氧化还原反应:
2KMnO4+10FeSO4+8H2SO4===2MnSO4+5Fe2(SO4)3+K2SO4+8H2O
设计如下原电池,其中甲、乙两烧杯中各物质的量浓度均为1 mol·L-1,盐桥中装有饱和K2SO4溶液。回答下列问题: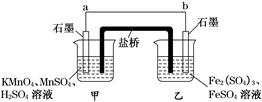
(1)发生氧化反应的烧杯是________(填“甲”或“乙”)。
(2)外电路的电流方向为:从________到________(填“a”或“b”)。
(3)电池工作时,盐桥中的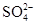 移向________(填“甲”或“乙”)烧杯。
移向________(填“甲”或“乙”)烧杯。
(4)甲烧杯中发生的电极反应为_________________________________________。