(10分)中学常见化学反应方程式为:A+B→X+Y+H2O(未配平,反应条件略去),其中,A、B的物质的量之比为1:4。请回答:
(1)若Y为黄绿色气体,该反应的离子方程式为 ,B体现出的化学性质有 。
(2)若A为常见的非金属单质,B的溶液为某浓酸,反应条件为加热,其反应的化学方程式为 。
(3)若A为某不活泼的金属单质,该反应能产生一种造成光化学烟雾(NO2)的气体,该反应中氧化剂与还原剂的物质的量之比为
(4)若A为常见的金属单质,常温下A在B的浓溶液中“钝化”,且A可溶于X溶液中。
写出A与X的溶液反应的离子方程式
(1)1mol氢气在氯气中充分燃烧生成氯化氢气体时放出184.6 kJ的热量,试写出对应的热化学方程式。标准状况下11.2L氢气在氯气中充分燃烧放出的热量是kJ。
(2)A(g)+B(g) C(g)+D(g)过程中的能量(kJ)变化如图所示,回答下列问题。
C(g)+D(g)过程中的能量(kJ)变化如图所示,回答下列问题。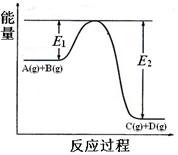
①反应物A(g)和B(g)具有的总能量(填大于、小于、等于)生成物C(g)和D(g)具有的总能量。
②该反应是_______反应(填吸热、放热),△H=(用E1和E2表示)。
③稳定性:反应物生成物(填大于、小于、等于)。
为了合理利用化学能,确保安全生产,化工设计需要充分考虑化学反应的焓变,并采取相应的措施。化学反应的焓变一般通过实验进行测定,也可进行理论推算。
(1)实验测得,0.3mol气态高能燃料乙硼烷(B2H6)在氧气中燃烧,生成固态三氧化二硼和液态水,放出649.5kJ热量。写出上述燃烧反应的热化学方程式。标准状况下11.2L乙硼烷完全燃烧生成液态水时放出的热量是kJ。
(2)在化学反应过程中,拆开化学键需要吸收能量,形成化学键又会释放能量。已知拆开1mol氢气中的化学键需要消耗436kJ能量,拆开1mol氧气中的化学键需要消耗496kJ能量,形成水蒸气中的1mol H-O键能够释放463kJ能量。试说明反应2H2(g)+O2(g)=2H2O(g)中的能量变化。
a=,b=。又知1mol液态水转化成气态水吸收44 kJ能量,则氢气完全燃烧生成液态水时的热化学方程式为。
(3)依据盖斯定律可以对某些难以通过实验直接测定的化学反应的焓变进行推算。实验中不能直接测出由石墨和氢气生成甲烷反应的反应热,但可测出CH4、石墨和H2燃烧热分别如下:
①CH4(g)+2O2(g)=CO2(g)+2H2O ΔH1=-890.3 kJ•mol-1
②C(石墨)+O2(g)= CO2(g) ΔH2= —393.5 kJ•mol-1
③H2(g)+ O2(g)=H2O(l) ΔH3= ─285.8 kJ•mol-1
O2(g)=H2O(l) ΔH3= ─285.8 kJ•mol-1
④C(石墨)+2H2(g)= CH4(g) ΔH4
试根据盖斯定律求出石墨生成甲烷的反应热ΔH4=。
(1)在下列物质中:①CO2 ②KOH ③Ne ④BaSO4 ⑤NaCl。
其中只含有离子键的是(填序号,下同),只含有共价键的是,
既含有离子键又含有共价键的是,不含化学键的是。
(2)下列物质在所述变化中:①食盐熔化 ②HCl气体溶于水 ③NH4Cl受热分解 ④干冰升华。
其中化学键未被破坏的是(填序号,下同),仅发生离子键破坏的是,
仅发生共价键破坏的是,既发生离子键破坏,又发生共价键破坏的是。
在25 ℃下,向浓度均为0.1 mol·L-1的MgCl2和CuCl2混合溶液中逐滴加入氨水,先生成____________沉淀(填化学式),生成该沉淀的离子方程式为________________。已知25 ℃时Ksp[Mg(OH)2] = 1.8×10-11,Ksp[Cu(OH)2] = 2.2×10-20。
现有A、B、C、D、E五种强电解质,它们在水中可电离产生下列离子(各种离子不重复)。
| 阳离子 |
H+、Na+、A13+、Ag+、Ba2+ |
| 阴离子 |
OH—、C1—、CO32—、NO3—、SO42— |
已知:①A、B两溶液呈碱性;C、D、E溶液呈酸性。
②A溶液与E溶液反应既有气体又有沉淀产生;A溶液与C溶液反应只有气体产生(沉淀包括微溶物,下同)。
③D溶液与另外四种溶液反应都能产生沉淀;C只能与D反应产生沉淀。
试回答下列问题:
(1)分别写出下列物质的化学式:A、B、E;
(2)写出A、E反应的离子方程式:;
(3)将C溶液逐滴加入等体积、等物质的量浓度的A溶液中,反应后溶液中各种离子浓度由大到小的顺序为:。
(4)已知:NaOH(aq)+HNO3(aq)=NaNO3(aq)+H2O(1);△H =-Q kJ·mol-1。
写出B与C稀溶液反应的热化学方程式。
(5)在100 mL 0.1 mol·L-1 E溶液中,逐滴加入40 mL 1.6 mol·L-1 NaOH溶液,最终得到沉淀物质的量为
mol。