(1)按官能团的不同,可以对有机物进行分类,请指出下列有机物的种类,填在横线上。
① CH3CH=CHCH3__________;② 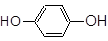 ___________;
___________;
③ 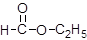 __________; ④
__________; ④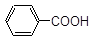 _____________;
_____________;
(2)按系统命名法命名
①CH3CH(C2H5)CH(CH3)2的名称___________________ ____
②(CH3)2C=C(CH3)2的名称______________________________
(20 分)有4种钠的化合物W、X、Y、Z,它们之间存在如下关系:
①W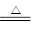 X+H2O+CO2↑②Z+CO2―→X+O2
X+H2O+CO2↑②Z+CO2―→X+O2
③Z+H2O―→Y+O2↑④X+Ca(OH)2―→Y+CaCO3↓
试回答下列问题:
(1)W、X、Y、Z的化学式分别是:W:______、X:______、Y:_______、Z:________。
(2)以上4个化学反应,属于氧化还原反应的是___________ (填反应序号),反应中氧化剂是__________ (写化学式),还原剂是__________ (写化学式)。
(3)若④反应在溶液中进行,写出其离子方程式以及能用该离子方程式表示的另一个化学反应的化学方程式:
①离子方程式:______________________________________________________。
②化学方程:_________________________________________________________。
(8 分)写出下列各离子反应方程式
(1)铝和氢氧化钠的反应
(2)氢氧化铝和盐酸的反应
(3)钠和盐酸的反应
(4)钠和硫酸铜的反应
(10 分)(1)明矾的组成为,明矾的用途,其在水中的电离方程式是。
(2)除去Na2CO3粉末中混入的NaHCO3杂质用 方法,化学方程式为 。
下列物质之间能够发生如下图所示的化学反应。合金由两种金属组成,取C溶液进行焰色反应,则火焰呈黄色。在反应中产生的水均未在图中标出。
(1)写出下列物质的化学式:
A,M,D,G。
(2)写出下列反应的化学方程式:
G→H。
M→D。
K→M。
(3)写出下列反应的离子方程式:
A→B+C。
K→D。
F→G 。
智利硝石矿层中含有碘酸钠,可用亚硫酸氢钠与其反应来制备单质,其化学反应式为:2NaIO3+5NaHSO3====3NaHSO4+2Na2SO4+I2+H2O
(1)反应中______________是氧化剂。
(2)用单线桥标出电子转移方向和数目
(3)从反应产物中,所得氧化产物与还原产物物质的量之比为___ _。