(1)合理利用二氧化碳,可以提高生活质量,促进工业发展。
①在常压下,-78 ℃时,二氧化碳气体凝结成固态二氧化碳,俗称干冰。某学生买回一盒冰淇淋月饼,盒里有很多作为致冷剂的碎干冰。下列关于干冰处理的正确做法是________。
A.将干冰放入冰箱
B.让干冰在通风处自然升华
C.直接将干冰倒入下水道
D.用手取干冰扔入废物箱
②在采煤工业上,把干冰与炸药放在一起,既能增强爆炸威力,又能防止火灾。能增强爆炸威力的原因是________________________________;能防止火灾的原因是______________________________________________________________________
________________________________________________________________________。
③使用传统催化剂,使二氧化碳与某些有机物反应可以生成塑料,但反应时间长。目前诞生的纳米级催化剂增加了催化剂的表面积,提高了____________________________。使用这种塑料能减少白色污染,因为它在微生物作用下,可以实现100%的________。
(2)目前,关于二氧化碳是否为大气污染物有不同的观点。认为“二氧化碳不是大气污染物”的理由是________。
①二氧化碳是重要的化工原料 ②二氧化碳是植物光合作用的必需原料 ③二氧化碳是无色、无味、无毒的气体
④除二氧化碳外,甲烷、一氧化二氮也是温室气体
A.①② B.②③
C.③④ D.①④
请将6种物质: N2O、FeSO4、Fe(NO3)3、HNO3和Fe2(SO4)3 H2O分别填入下面对应的横线上,组成一个未配平的化学方程式:
(1)方程式为:+→+ + +
(2)反应物中发生氧化反应的物质是,被还原的元素是。
(3)反应中1mol氧化剂发生还原时转移电子数为mol
(4)配平后的系数填入下列相应的空格上
Ⅰ.已知:R-CH=CH-O-R′ 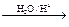 R-CH2CHO + R′OH
R-CH2CHO + R′OH
(烃基烯基醚)
烃基烯基醚A的相对分子质量(M r)为176,分子中碳氢原子数目比为3∶4。与A相关的反应如下: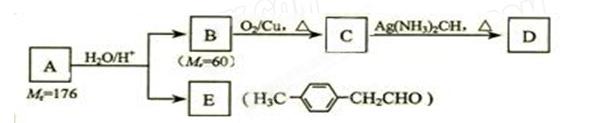
请回答下列问题:
⑴ A的分子式为_________________。
⑵写出C → D反应的化学方程式:____________________________________。
⑶写出两种同时符合下列条件的E的同分异构体的结构简式:______________、___________________。
① 属于芳香醛; ② 苯环上有两种不同环境的氢原子。
Ⅱ.由E转化为对甲基苯乙炔(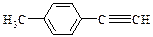 )的一条路线如下:
)的一条路线如下: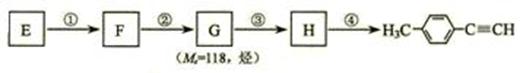
⑷写出G的结构简式:____________和第④步反应的条件_ ___________________。
___________________。
乳酸分子式为C3H 6O3,在一定的条件下可发生许多化学反应,下图是采用化学方法对乳酸进行加工处理的过程。其中A、H、G为链状高分子化合物,已知F常做内燃机的抗冻剂。
6O3,在一定的条件下可发生许多化学反应,下图是采用化学方法对乳酸进行加工处理的过程。其中A、H、G为链状高分子化合物,已知F常做内燃机的抗冻剂。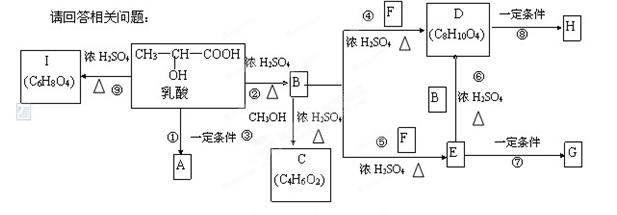
(1)请 写出C结构简式为;A的名称为。
写出C结构简式为;A的名称为。
( 2)B中所含的官能团名称;反应⑦的反应类型是。
2)B中所含的官能团名称;反应⑦的反应类型是。 (3)反应④的化学方程式为。
(3)反应④的化学方程式为。
(4)反应⑨的化学方程式为。
请按下列要求填空
(1)支链上只有一个乙基,且式量最小的烷烃的名称。
(2)将甘氨酸(H2N-CH2-COOH)和丙氨酸( )缩合最多可形成____种二肽。
)缩合最多可形成____种二肽。
(3)有机物X的键线式(如右图所示)。
另一有机物Y是X的同分异构体,且属于芳香烃,请写出Y与乙烯在一定条件下发生聚合反应的化学方程式:。
某有机物 A结构如右图所示,取Na、NaOH、H2在一定条件下分别与等物质的量的A充分反应,理论上需要上述三种物质的物质的量之比为__________。
A结构如右图所示,取Na、NaOH、H2在一定条件下分别与等物质的量的A充分反应,理论上需要上述三种物质的物质的量之比为__________。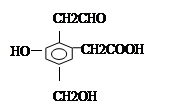
工业合成氨是硝酸工业中的重要步骤,已知N2(g) +3H2(g)  2NH3(g)ΔH=-92.4kJ·mol-1。请回答:
2NH3(g)ΔH=-92.4kJ·mol-1。请回答:
(1) 当合成氨反应达到平衡后,改变某一外界条件(不改变N2、 H2和NH3的量),反应速率与时间的关系如右图所示。
H2和NH3的量),反应速率与时间的关系如右图所示。
图中t1时引起平衡移动的条件可能是 __,t3时引起平衡移动的条件可能是 __ ___, 其中表示平衡混合物中NH3的含量最高的一段时间是。
(2) 温度为T ℃时,将2a mol H2和a mol N2放入0.5L密闭容器中,充分反应后测得N2的转化率为50﹪。则该反应的化学平衡常数的值为 ___________________。请在答题卷上写出具体的计算过程。