工业合成氨是硝酸工业中的重要步骤,已知N2(g) +3H2(g)  2NH3(g) ΔH=-92.4kJ·mol-1。请回答:
2NH3(g) ΔH=-92.4kJ·mol-1。请回答:
(1) 当合成氨反应达到平衡后,改变某一外界条件(不改变N2、 H2和NH3的量),反应速率与时间的关系如右图所示。
H2和NH3的量),反应速率与时间的关系如右图所示。
图中t1时引起平衡移动的条件可能是 __ , t3时引起平衡移动的条件可能是 __ ___ , 其中表示平衡混合物中NH3的含量最高的一段时间是 。
(2) 温度为T ℃时,将2a mol H2和a mol N2放入0.5L密闭容器中,充分反应后测得N2的转化率为50﹪。则该反应的化学平衡常数的值为 ___________________。请在答题卷上写出具体的计算过程。
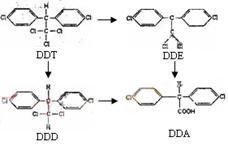
⑴分子中所有原子可以处于同一平面的有 (选填“DDT、DDE、DDD、DDA”)。
⑵DDA中所含的官能团,除苯环外,还有
⑶指出下列有机反应类型:①DDT→DDE 反应;②DDE→DDD 反应
⑷若在实验室也可实现由DDT→—DDE,试写出该反应的化学方程式:
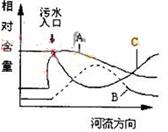
请回答有关问题:
⑴图中绘出的三种曲线分别代表氮、磷等无机盐总量,水中氧
气溶解量(DO),有机物溶解量,其中表示水中DO变化曲
线的是 (选填A、B、C、D)
⑵目前推广使用无磷洗衣粉,并提倡科学合理施用化肥,其目的是防止水体
(填与环境相关的术语)。
⑶某研究性学习课题小组拟调查测定本地区水质污染情况,如
果你是课题小组成员,现要取三份不同地区的水样,你选择的三个地点是:
① ② ③ ⑷氨在水体中化学降解时,是水体中两种不同的硝化细菌分两步,将其逐步氧化的,过程如下:,某同学在该地工业园区取得水样,准备检测其中无机氮的含量,查阅工具书后,决定先检测水样中的铵或氨的浓度,反应原理为2K2[HgI4]+NH4Cl+4KOH==(OHg2NH2)I(红色)+KCl+7KI+3H2O,用比色法测定。
⑷氨在水体中化学降解时,是水体中两种不同的硝化细菌分两步,将其逐步氧化的,过程如下:,某同学在该地工业园区取得水样,准备检测其中无机氮的含量,查阅工具书后,决定先检测水样中的铵或氨的浓度,反应原理为2K2[HgI4]+NH4Cl+4KOH==(OHg2NH2)I(红色)+KCl+7KI+3H2O,用比色法测定。
①比色法能测定其中NH3—NH4+的浓度,原理是
②若测得的含量异常偏高,再用其他方法测得NO2—和NO3—含量略偏高。可能的原因是
A、可能是硝酸工厂大量排出的含硝酸的废水
B、合成氨厂,刚排放的溶有氨的废水
C、造纸厂排出的有机废水和合成氨厂排出的溶有氨的废水
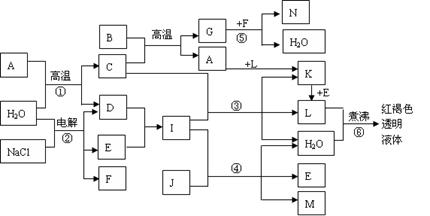
⑴写出化学式:B: ;L:
⑵写出反应方程式①
④
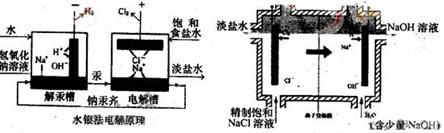
⑶反应②在上世纪七十年代常用水银法替代生产,此法通过钠汞齐(Na·nHg)生产得到的烧碱质量号,浓度高,目前已被离子交换膜法所取代。两种生产方法示意图如下:
下列说法肯定不正确的是 (选填A、B、C、D)
A、水银法被淘汰,可能是时汞毒性大,易造成环境污染
B、水银法在电解槽中,阴极的电极反应式为:Na++e—+nHg== Na·nHg
C、离子膜法电解,阳极发生的电极反应为2H+ + 2e— = H2
D、离子膜法烧碱在阴极生成,水银法烧碱在解汞槽中生成
⑴2006年11月16日美国和俄罗斯科学家联合宣布,他们合成出了118号元素,新原子的质量数为297,则该新原子中子数与质子数之差为
⑵人们研究发现第一周期与第二周期一些元素性质与同族元素性质共性很少,有人建议将氢放在ⅦA,写出一种能支持该观点的化合物:,人们发现Li+溶剂化倾向和形成共价键倾向很强,提出类似氢键的“锂键”,请写出(LiF)2含锂键的结构式:
⑶研究周期表发现存在对角线规则,处在对角线上的元素性质相似,如硼和硅处于对角线,请写出硼和氢氧化钠溶液反应的离子方程式:
⑴配平反应器中发生的反应方程式:
I2 + KIO3 + H2O="=" KH(IO3)2 + KCl + Cl2↑
⑵步骤②中,用硝酸而不用HI,其原因可能是
⑶步骤③要保持溶液微沸1小时,以完全排出氯气,排出氯气的原因为
⑷合成实验中涉及两次过滤,在实验室进行过滤实验时,用到的玻璃仪器有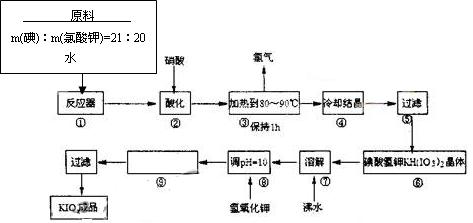
⑸用氢氧化钾调节溶液的PH值,发生的反应方程式为:
⑹参照碘酸钾溶解度曲线,步骤得到碘酸钾晶体,你建议的方法是
| 温度 |
0 |
10 |
20 |
40 |
60 |
80 |
| KIO3g/100g水 |
4.60 |
6.27 |
8.08 |
12.6 |
18.3 |
24.8 |