下列溶液中溶质的物质的量浓度为1mol/L的是( )
| A.将58.5gNaCl溶解在1L水中 |
| B.将1L10mol/L的浓盐酸加入9L水中 |
| C.将22.4LHCl气体溶于水配成1L溶液 |
| D.将10gNaOH溶解在少量水中,再加蒸馏水直到溶液体积为250mL |
下列实验操作能达到预期实验目的的是
| 实验目的 |
实验操作 |
|
| A |
鉴别CO32-和 SO42- |
分别加入饱和CaCl2溶液 |
| B |
比较Al和Fe的金属活动性 |
分别加入浓NaOH溶液 |
| C |
比较苯酚和乙酸的酸性 |
分别加入NOH溶液 |
| D |
比较AgCl和AgI的溶解度 |
向AgCl的饱和液中加少量KI溶液 |
下列各组离子在碱性条件下能大量共存,而在强酸性条件下能发生氧化还原反应的是
| A.Mg2+、Na+、SO42-、Cl— |
| B.K+、CO32-、Cl—、NO3— |
| C.NH4+、Na+、SO42-、NO3— |
| D.Na+、K+、NO3—、SO32— |
设NA为阿伏加德罗常数的值,下列叙述中正确的是
A.标准状况下,1.8 g H2O所含有的质子数为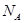 |
B.1 L 1 mol/L的Na2CO3溶液中含有的CO32-数目为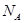 |
C.25℃时,1 L pH=13的 Ba(OH)2溶液中含有的OH-数目为0.2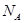 |
D.标准状况下,2.24 L 氯气与过量的氢氧化钠溶液完全反应转移的电子数为0.2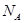 |
在短周期中,R原子最外层电子数是其次外层电子数的3倍,下列说法不正确的是
| A.原子半径大小:X>Y>Z |
| B.氢化物的稳定性:X>Y |
| C.化合物YR2能使品红溶液褪色 |
| D.X、Y、Z三种元素最高价氧化物的水化物的酸性最强的是Z |
菜谱中记载:河虾不宜与西红柿同食。主要原因是河虾中含有五价砷,西红柿中含有比较多的维生素C,两者同食时会生成有毒的+3价砷。下列说法中正确的是
| A.在该反应中维生素C作催化剂 |
| B.因为河虾中含有砷元素,所以不能食用 |
| C.砒霜是砷的氧化物,由上述信息可推知砒霜中含有的砷可能是+3价砷 |
| D.上述反应中维生素C作氧化剂 |