能正确表示下列化学反应的离子方程式的是( )
A.碳酸钙和盐酸反应:CO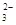 +2H+ +2H+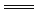 H2O+CO2↑ H2O+CO2↑ |
| B.铜片插入硝酸银溶液中:Cu + Ag+=Cu2+ + Ag |
C.向稀硫酸溶液中加铁:3Fe+6H+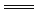 3Fe3++3H2↑ 3Fe3++3H2↑ |
| D.氧化镁与稀硝酸混合: MgO+2H+=Mg2++H2O |
某气态烃1mol和2mol氯化氢发生加成反应后,最多还能和6mol氯气发生取代反应。由此可以断定原气态烃是(气体体积均在相同条件下测定)()
| A.乙炔 | B.丙炔 | C.丁炔 | D.丁二烯 |
A、B两种烃,它们的最简式相同,下列关于A和B的叙述正确的是()
A.A和B一定是同分异构体B.A和B的摩尔质量一定相同
C.A和B一定具有相同化学性质 D.A和B可能不是同系物
已知0.1mol·L-1的二元酸H2A溶液的pH=4,则下列说法中正确的是()
A.在Na2A、NaHA两溶液中,离子种类不相同
B.在溶质物质的量相等的Na2A、NaHA两溶液中,阴离子总数相等
C.在NaHA溶液中一定有c(Na+)+c(H+)=c(HA-)+c(OH-)+2c(A2-)
D.在Na2A溶液中一定有c(Na+)>c(A2-)>c(H+)>c(OH-)
某有机物在氧气中充分燃烧,生成等物质的量的水和二氧化碳,则该有机物必须满足的条件是()
A.分子中C、H个数比为1:2 B.分子中的C、H、O的个数比为1:2:3
C.该有机物的相对分子质量为14 D.该分子中肯定不含氧元素
干洗衣服的干洗剂主要成分是四氯乙烯,家用不粘锅内侧涂覆物质的主要成分是聚四氟乙烯。下列关于四氟乙烯和聚四氟乙烯的说法正确的是 ( )
| A.它们都是纯净物 |
| B.它们都能是酸性高锰酸钾溶液褪色 |
| C.它们的分子中都不含氢原子 |
| D.它们都可由乙烯只发生加成反应得到 |