用2.4 mol/L的H2SO4溶液配制100mL浓度为0.2 mol/L的稀H2SO4,回答下列问题:
(1)需用量筒量取2.4 mol/L的H2SO4溶液的体积是 mL。
(2)溶液配制的所需的基本步骤如下:
将上述实验步骤A到F按实验过程先后次序排列___________________ 。
(3)上述实验步骤A、B、E、F都用到的仪器名称为__________。
(4)取上述所配溶液10mL与足量BaCl2溶液反应,生成白色沉淀0.48 g。则该溶液
浓度 0.2 mol/L(填“大于”“等于”或“小于”),造成此误差的操作可能
是 。
a. 定容时俯视容量瓶; b. 用量筒取2.4 mol/LH2SO4溶液时俯视读数;
c. 容量瓶使用前未干燥;d. 使用的烧杯和玻璃棒未洗涤彻底;
e. 定容时将蒸馏水洒在容量瓶外面
A~D是中学化学实验中使用温度计的装置示意图,其中所做实验与装置不相符的是:
| 序号 |
A |
B |
C |
D |
||
| 装置 |
 |
 |
 |
|
||
| 实验 |
乙烯的制取 |
石油的分馏 |
银镜反应 |
苯的硝化 |
下图为配制0.2mol·L-1Na2CO3溶液250mL示意图。
回答下列问题:
(1)①中称得Na2CO3_____________g。
(2)玻璃棒在②、③两步中的作用分别是_____________、_____________。
(3)若出现如下情况,对所配溶液浓度有何影响?(填“偏高”、“偏低”或“无影响”)
A.某同学在第⑧步观察液面时俯视_____________;
B.没有进行操作步骤④和⑤_____________;
C.在第⑤步不慎有少量液体流到容量瓶外_____________。
为了测定某烷烃样品(丁烷,并含少量丙烷等气态烃)的平均式量,设计了下面的实验:
①取一个配有合适胶塞的洁净、干燥的锥形瓶,准确称量,得到质量m1
②往锥形瓶中通入干燥的该烷烃样品,塞好胶塞,准确称量,重复操作,直到前后两次称量结果基本相同,得到质量m2
③往锥形瓶内加满水,塞好胶塞,称量得到质量m3
已知实验时的温度t(K),压强p(kPa),水的密度ρ水(g·L-1),空气的平均式量29.0、密度ρ空气(g·L-1)
回答下列问题:
(1)本实验的原理是(具体说明)什么?
(2)步骤②中为什么要重复操作,直到前后两次称量结果基本相同?
(3)具体说明本实验中怎样做到每次测量都是在相同体积下进行的?
(4)本实验中收集气体样品的操作,可选用的方法是(填图中标号)。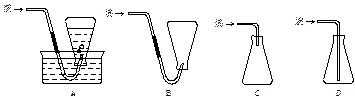
图3—2
(5)锥形瓶内空气的质量(m空气)是(列出算式)。
(6)瓶中样品的质量(m样品)是(列出算式)。
(7)由实验测得烷烃的平均式量是(列出算式)。
用18mol/L的硫酸配制100mL 1.0mol/L硫酸,若实验仪器有:
A.100mL量筒 B.托盘天平 C.玻璃棒 D.50mL容量瓶
E.10mL量筒 F.胶头滴管 G.50mL烧杯 H.100mL容量瓶
(1)实验时应选用仪器的先后顺序是(填入编号)。
(2)在容量瓶的使用方法中,下列操作不正确的是(填写标号)。
A.使用容量瓶前检查它是否漏水。
B.容量瓶用蒸馏水洗净后,再用待配溶液润洗。
C.配制溶液时,如果试样是固体,把称好的试样用纸条小心倒入容量瓶中,缓慢加入蒸馏水到接近标线1cm~2cm处,用滴管滴加蒸馏水到标线。
D.配制溶液时,如果试样是液体,用量筒量取试样后直接倒入容量瓶中,缓慢加入蒸馏水到接近标线1cm~2cm处,用滴管滴加蒸馏水到标线。
E.盖好瓶塞,用食指顶住瓶塞,用另一只手的手指托住瓶底,把容量瓶倒转和摇动多次。
某种常见金属的部分性质如下:银白色固体,硬度较小,密度为2.70g/cm3,熔点为660.4℃,导电性、导热性、延展性良好。
(1)试推断该金属可能的一种用途______。
(2))请提出你想探究的有关该金属化学性质的两个问题:①______;②______。
(3)请设计实验方案对你所提出的两个问题进行探究(简述步骤、现象及结论):
①__________________________;②__________________________。