设NA为阿伏伽德罗常数,下列说法中正确的是( )
| A.0.1mol过氧化钠固体中含阴离子个数为0.2NA |
| B.1mol金刚石中含C-C的数目为4NA |
| C.标准状况下,22.4L乙炔中含π键数为2NA |
| D.1molNaHSO4晶体中阳离子数为2NA |
在某密闭容器中,可逆反应:A(g)+B(g)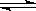 xC(g),符合下列图像(Ⅰ)所示关系。由此推断对图像(Ⅱ)的正确说法是
xC(g),符合下列图像(Ⅰ)所示关系。由此推断对图像(Ⅱ)的正确说法是

| A.P3﹥P4 , y轴表示A的百分含量 |
| B.P3﹤P4 , y轴表示B的百分含量 |
| C.P3﹤P4 , y轴表示混合气体的密度 |
D.P3﹥P4 , y轴表示混合气体的 平均相对分子质量 平均相对分子质量 |
恒温、体积为1L的密闭容器中,充入2molPCl3和1molCl2发生下述反应:
PCl3 (g)+ Cl2(g) 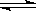 PCl5 (g)
PCl5 (g)
达到平衡时,PCl5为0.4mol。如果从体系中移走1molPCl3和0.5molCl2,重新达到平衡时,PCl5的物质的量为
| A.0.15 mol | B.0.2 mol | C.0.24 mol | D.0.48 mol |
某温度下在密闭容器中发生如下反应:2M(g)+ N(g) 2E(g),若开始时只充入2 mol E气体,达到平衡时,混合气体的压强比起始增大了20%;若开始时只充入了3 mol M和1 mol N的混合气体,达到平衡时M的转化率为
2E(g),若开始时只充入2 mol E气体,达到平衡时,混合气体的压强比起始增大了20%;若开始时只充入了3 mol M和1 mol N的混合气体,达到平衡时M的转化率为
| A.<60% | B.=40% | C.<40% | D.>60% |
电解硫酸铜溶液时,要求满足下列三点要求:①阳极质量逐渐减少;②阴极质量逐渐增加;③电解液中铜离子浓度不变。根据这三点要求可以选用的电极是
| A.石墨作阴极,纯铜作阳极 |
| B.含有锌、银的铜合金作阴极,石墨作阳极 |
| C.纯铁作阳极,纯铜作阴极 |
| D.含有锌、银的铜合金作阳极,纯铜作阴极 |
已知某可逆反应,x A(g)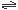 y B(g),平衡时测得A的浓度为0.5 mol/L,保持温度不变,将容器体积扩大到原来的两倍,再达到平衡时,测得A的浓度为0.3 mol/L。下列判断正确的是
y B(g),平衡时测得A的浓度为0.5 mol/L,保持温度不变,将容器体积扩大到原来的两倍,再达到平衡时,测得A的浓度为0.3 mol/L。下列判断正确的是
| A.x < y | B.平衡向正反应方向进行 |
| C.B的体积分数降低 | D.缩小体积、增大压强,A的体积分数增大 |