为了除去氯化镁酸性溶液中的Fe3+,可在加热搅拌的条件下加入一种过量的试剂,过滤后再加入适量的盐酸。这种试剂( )
| A.氨水 | B.氢氧化钠 | C.碳酸钠 | D.碳酸镁 |
下列关于氯气的叙述中,不正确的是
| A.氯气是一种黄绿色、有刺激性气味的气体 |
| B.氯气能溶于水 |
| C.氯气、液氯、氯水是同一种物质 |
| D.氯气是一种有毒的气体 |
物质的量相同的下列物质中,含原子数最多的是
| A.O2 | B.CH4 | C.CO | D.NH3 |
下列化学反应中,属于置换反应的是
| A.NaOH + HCl ===NaCl + H2O |
B.H2+CuO 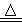 Cu + H2O Cu + H2O |
C.Fe2O3 +3CO 2 Fe + 3CO2 2 Fe + 3CO2 |
D.2CO + O2 2CO2 2CO2 |
同种类型的物质往往具有某些相同的性质。下列性质中不属于酸通性的是
| A.使紫色石蕊试液变蓝色 |
| B.与碱反应生成盐和水 |
| C.与活泼金属反应生成盐和氢气 |
| D.与氧化钠反应生成盐和水 |
将下列各组物质按单质、氧化物、酸、碱、盐分类顺序排列,其中正确的是
| A.镁、干冰、硫酸、纯碱、食盐 |
| B.碘酒、冰、盐酸、烧碱、硫酸钡 |
| C.氢气、氧化钠、硝酸、烧碱、氯化铜 |
| D.铁、氧化铜、醋酸、石灰水、硝酸钾 |