下列各组离子在所给条件下能够大量共存的是( )
| A.pH =0的溶液中:Fe3+、Mg2+、Cl-、SO42- |
| B.水电离出的c(H+)=1×10—13mol/L的溶液中: K+、HCO3-、Cl-、S2- |
| C.使pH试纸显深蓝色的溶液中:Cu2+、NO3-、Fe3+、SO42- |
| D.在AlCl3溶液中:Na+、AlO2-、NO3-、SO42- |
下列各组物质所发生的化学反应中,由于反应物的用量不同而得到不同产物的是
①铁与稀硝酸②硫酸铜溶液与氨水③碳酸钠溶液与稀盐酸④铁与氯气
| A.①②③ | B.①②③④ | C.②③ | D.③④ |
下列叙述错误的是
| A.Al2(SO4)3可除去酸性废水中的悬浮颗粒 |
| B.氯气与石灰乳反应能得到含氯漂白剂 |
| C.燃煤时加入适量石灰石,可减少废气中SO2的排放 |
| D.工业上硝酸可用于制化肥、农药、炸药和染料等 |
有一未知的无色溶液,只可能含有以下离子中的若干种(忽略由水电离产生的H+、OH-):H+、NH4+、K+、Mg2+、Cu2+、Al3+、NO3-、CO32-、SO42-,现取三份100mL溶液进行如下实验:
①第一份加足量AgNO3溶液后,有白色沉淀产生。
②第二份加足量BaCl2溶液后,有白色沉淀产生,经洗涤、干燥后,沉淀质量为6.99 g。[
③第三份逐滴滴加NaOH溶液,测得沉淀与NaOH溶液的体积关系如图。根据上述实验,以下推测不正确的是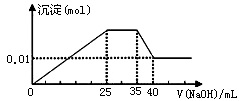
| A.原溶液一定不存在H+、Cu2+、CO32- |
| B.不能确定原溶液是否含有K+、NO3- |
| C.原溶液确定含Mg2+、Al3+、NH4+,且n(Mg2+):n(Al3+):n( NH4+)=1:1:2 |
| D.实验所加的NaOH的浓度为2mol·L-1 |
下列说法正确的是
| A.已知Ag2CrO4的Ksp为1.12×10-12,则将等体积的1×10-3mo1/L的AgNO3溶液和1×0-3mo1/LK2CrO4溶液混合,会有Ag2CrO4沉淀产生 |
| B.Si—O键的键能大于Si—Cl键的键能,因此SiO2的熔点高于晶体SiCl4的熔点 |
| C.常温时,浓度均为0.01mol/L Na2CO3溶液和NaHCO3溶液,等体积混合,其溶液中粒子浓度关系为3c(Na+)=2c(HCO3-)+2c(CO32-)+2c(H2CO3) |
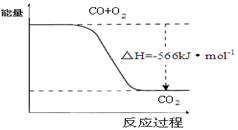
| D.已知:2CO(g)+O2(g)=2CO2(g) △H=-566kJ·mol-1,下图可表示由CO生成CO2的反应过程和能量关系 |
某汽车尾气分析仪以燃料电池为工作原理测定CO的浓度,其装置如图所示(上端为多孔电极a,下断为多孔电极b),该电池中电解质为氧化钇-氧化钠,其中O2-可以在固体介质NASICON中自由移动。下列说法不正确的是
| A.工作时电极b作正极,O2-由电极b流向电极a |
| B.工作时电子由电极a通过介质流向电极b |
| C.负极的电极反应式为:CO+O2—―2e-=CO2 |
| D.传感器中通过的电流越大,尾气中CO的含量越高 |