实验室制取气体所需装置如下图所示,请回答以下问题: 
(1)图中标示仪器的名称(1) ,(2) 。
(2)实验室选用B和E装置可以制取的气体是 ,一般不用c装置收集CO2的原因是
。不选用D装置收集CO2的原因是 ,实验室如选用G装置收集二氧化碳,气体应该从 端进入。
(3)用高锰酸钾制取氧气时,选用的发生装置是 ,反应的化学方程式为 。如果要制得较纯净的氧气应该选择装置 收集。
(5分)钢铁的冶炼是人类文明的一个重要标志。图1是实验室模拟炼铁的装置图。


图一图二图三
(1)写出图1中A处发生的化学反应方程式:;
(2)实验过程中通入CO质量与红色粉末质量的关系如图2所示。根据图示,下列说法不正确的是;(填序号)
①a点表示开始通入CO,反应开始发生
②b点表示通入CO一段时间后加热,反应开始发生
③c点表示红色粉末已充分参加反应
④d点表示反应结束后仍需继续通入CO
⑤可根据通入CO的质量计算出红色粉末的质量
(3)图1装置中的不足之处是。
(4)该实验炼制的铁与工业炼制出的铁最大的区别是。
(5)某化学小组的同学们利用上述实验对一份固体样品进行了探究。通过实验已确定该样品由氧化铁和铁粉混合而成。他们取了3.6g固体样品,用图1所示的装置重新实验,测定的部分数据如图3所示,则原样品中铁元素与氧元素的质量比是。
(6分) 根据下列装置图,按要求回答有关问题: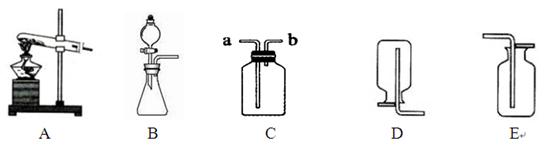
(1)实验室制取二氧化碳的发生装置是(填字母),反应的化学方程式为。
(2)若选用右图装置收集二氧化碳气体时,气体应从端进。如何检验该气体(用化学方程式表示)。 
(3)实验室常用加热氯化铵与碱石灰固体混合物的方法来制取氨气(NH3),则制取氨气的发生装置应选用(填字母)。收集氨气的装置只能用D,而不能用C或E。由此可知氨气应具有的性质是。
(4分) 某化学小组围绕燃烧与灭火的主题开展了相关活动。请你参与完成: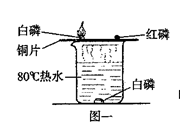
(1)从图一中观察到的现象及所得到结论正确的是。
A.实验中烧杯里的热水只起提高温度的作用
B.水下白磷未燃烧是由于没有与氧气接触
C.实验不能比较白磷和红磷的着火点高低
D.实验说明可燃物燃烧时,温度必须达到着火点或与氧气接触
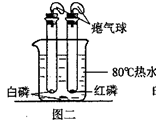
(2)改进后的装置(如图二)与图一相比,其优点是。欲使图二中的红磷着火,可将试管从水中取出并后才能对试管加热。
(3) 学习化学的目的并不在于要成为化学家,重要的是善于用化学知识去分析、解决生产生活中的问题。从化学的角度看,下列做法中不正确的是。
A.家用电器着火,应先切断电源再用泡沫灭火器灭火
B.油锅着火,应迅速向锅中掺水,降低温度使其熄灭
C.大楼里着火时,应该用湿毛巾捂住口鼻,俯下身子逃出火灾区
D.室内起火时,应打开门窗,避免吸入浓烟
E.森林失火,向逆风方向奔跑逃离火灾区
(10分)在研究“铁生锈的条件及防治”的实验中,某兴趣小组对实验进行了创新设计,请把实验报告补充完整。
《实验目的》铁生锈条件的探究。
《实验内容》取3段光亮无锈的细铁丝,绕成螺旋状,放入3支干燥洁净的试管底部,进行下列实验,实验要保证有足够长的时间来观察现象。
实验①实验②实验③
《实验现象》实验①②无明显现象,实验③中铁丝生锈,且试管内空气体积减小。
《实验结论》铁生锈实际上是铁与空气中的、(填名称)发生反应的结果。
《实验思考》
(1)当铁丝足量,时间足够长,实验③进入试管内的水的体积约占试管体积的。
(2)该实验创新之处在于:可根据铁丝表面的铁锈和两种现象来判断铁丝反应进行的情况。
(3)用完的菜刀要擦干存放,理由是。
(4)铝比铁活泼,但铝难腐蚀,原因是。
(5)为了防止钢铁锈蚀,人们常将铁制成不锈钢,不锈钢属于__________(填“纯净物”或“混合物”)。此外还可以采用在铁器表面涂刷矿物油或镀上其他金属等覆盖保护膜的方法,此方法能防止锈蚀的原理是__ _ ____。
(6)媒体报道每年因生锈而浪费的钢铁非常严重,请你用方程式表达如何用稀硫酸处理铁锈(Fe2O3)。
两瓶失去标签的无色溶液,分别是盐酸和氢氧化钠溶液,请用合适的方法鉴别出来。
| 操作方法 |
实验现象 |
结论 |