(10分)在研究“铁生锈的条件及防治”的实验中,某兴趣小组对实验进行了创新设计,请把实验报告补充完整。
《实验目的》铁生锈条件的探究。
《实验内容》取3段光亮无锈的细铁丝,绕成螺旋状,放入3支干燥洁净的试管底部,进行下列实验,实验要保证有足够长的时间来观察现象。
实验① 实验② 实验③
《实验现象》实验①②无明显现象,实验③中铁丝生锈,且试管内空气体积减小。
《实验结论》铁生锈实际上是铁与空气中的 、 (填名称)发生反应的结果。
《实验思考》
(1)当铁丝足量,时间足够长,实验③进入试管内的水的体积约占试管体积的 。
(2)该实验创新之处在于:可根据铁丝表面的铁锈和 两种现象来判断铁丝反应进行的情况。
(3)用完的菜刀要擦干存放,理由是 。
(4)铝比铁活泼,但铝难腐蚀,原因是 。
(5)为了防止钢铁锈蚀,人们常将铁制成不锈钢,不锈钢属于__________(填“纯净物”或“混合物”)。此外还可以采用在铁器表面涂刷矿物油或镀上其他金属等覆盖保护膜的方法,此方法能防止锈蚀的原理是__ _ ____。
(6)媒体报道每年因生锈而浪费的钢铁非常严重,请你用方程式表达如何用稀硫酸处理铁锈(Fe2O3) 。
【2015年湖北省十堰市】某学习小组探究氢氧化钙溶液的化学性质,并作了延伸探究。
探究一:甲同学设计了如下实验方案,请你帮助完成实验报告。
【提出问题】实验方案(3)褪色后溶液中的溶质是什么?
【查阅资料】氯化钙溶液呈中性。
【作出猜想】乙同学从反应情况分析,溶液中除含少量酚酞外,溶质可能有以下三种情况:
①氯化钙 ②氯化钙和氯化氢 ③氯化钙和氢氧化钙
【分析讨论】丙同学从实验现象分析得出:猜想③肯定不合理,其理由是 。
探究二:丁同学为进一步验证乙同学的猜想,设计实验如下:将实验方案(3)褪色后溶液倒入烧杯中,向其中逐滴滴加稀碳酸钠溶液至过量,边滴加边振荡。实验后得出产生沉淀质量与碳酸钠溶液体积之间的关系,如图所示。写出实验过程中的现象 。
【得出结论】乙同学的猜想中, (填序号)合理。
【反思讨论】学习小组结合图像,分析了丁同学实验过程中烧杯内溶液的变化。下列说法正确的是 。(填序号)
| A.溶液质量逐渐增大 | B.氯化钠质量逐渐增大,V2后不变 |
| C.氯化钙的质量先增大后减小 | D.溶液的pH一直增大 |
【2015年辽宁省丹东市】为探究氢氧化钙溶液和稀盐酸反应所得溶液中溶质的成分,小鸣和同学们通过测定了反应后溶液的pH,得到了如右图所示的pH曲线,请回答:
(1)由图可知该实验操作是将 滴加到另一种溶液中;
(2)该反应的化学方程式为 ;
(3)实验过程中,小鸣取了a、b、c三处反应后的溶液于三个烧杯中,却忘了作标记,请你设计不同的方案(不再用测定pH的方法),探究三种样品分别属于哪处溶液。
【查阅资料】CaCl2溶液显中性,CaCl2+Na2CO3=CaCO3↓+2NaCl。
【探究过程】
①分别取少量样品于三支试管中,加入酚酞试液,观察到其中一支试管内出现 的现象。结论:该样品是a处溶液。
②为进一步确定b或c处溶液,又设计了以下方案:
| 实验步骤 |
实验现象 |
实验结论 |
| 另取余下样品少量于两支试管中,分别滴加足量的Na2CO3溶液。 |
该样品为b处溶液。 |
|
| 该样品为c处溶液,并推知溶液中的阳离子有 。 |
【反思评价】探究反应后溶液中溶质的成分,除了要考虑生成物之外,还要考虑 。
【2015年陕西省】下图是甲、乙两位同学一起在实验室进行的氢氧化钠与盐酸中和反应的实验。
(说明:图中A1、A2、A3、B1、B2、B3均为溶液编号)
根据上图实验,请你与甲、乙同学一起完成下列探究:
| 探究环节 |
甲同学的探究 |
乙同学的探究 |
| 提出问题 |
A3溶液为什么不变红? |
B3溶液中溶质成分是什么?(酚酞不计) |
| 作出猜想 |
实验过程中,酚酞变质了。 |
猜想一:NaCl猜想二:NaCl、HCl |
| 实验验证 |
(1)取少量A3溶液于另一试管中,向其中滴加NaOH溶液,溶液变红,说明甲同学的猜想 (填“成立”或“不成立”)。 (2)你认为,在常温下A2溶液测出的pH应 (填“>”、“=”或“<”)7。 |
取少量B3溶液加入盛有少量铁粉的试管中,观察到有无色气泡产生,固体逐渐减少,溶液由无色变为 。据此,你认为乙同学的猜想 (填“一”或“二”)成立。 |
| 交流反思 |
(1)甲、乙同学的实验中,反应均涉及到的化学方程式是 。 (2)A3溶液未变红,你认为原因是A2溶液中 较多,加入的NaOH溶液未将其完全中和。 (3)甲、乙同学经过实验对比探究,一致认为做化学实验时应注意药品用量的控制。 |
【2015年北京市】众所周知,酚酞溶液遇 溶液变红。但是,在分组实验中(如右图所示),出现了意想不到的现象:有的溶液变红后褪色;有的出现白色浑浊物。
溶液变红。但是,在分组实验中(如右图所示),出现了意想不到的现象:有的溶液变红后褪色;有的出现白色浑浊物。
【提出问题】分组实验中,出现意想不到的现象的原因是什么呢?
【查阅资料】酚酞溶液由酚酞固体溶于酒精配制而成。
【猜想与假设】
Ⅰ.红色褪去,与 溶液和空气中的
溶液和空气中的 反应有关。
反应有关。
Ⅱ.红色褪去,与NaOH溶液的浓度有关。
Ⅲ.出现白色浑浊物,与酚酞溶液的浓度有关。
【进行实验】
| 实验 |
实验操作 |
实验现象 |
|
| 1 |
向盛有2mL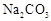 溶液的试管中滴加5滴0.5%的酚酞溶液 溶液的试管中滴加5滴0.5%的酚酞溶液 |
溶液变红 |
|
| 2 |
 |
1号试管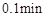 红色褪去 红色褪去2号试管5min红色褪去 3号试管30min红色明显变浅 4号试管120min红色无明显变化 |
|
| 3 |
取3支试管,分别加入2mL水,…… |
酚酞溶液浓度/% |
浑浊程度 |
| 5 |
大量浑浊物 |
||
| 2 |
少量浑浊物 |
||
 |
无浑浊物 |
【解释与结论】
(1) 与
与 反应的化学方程式为 。
反应的化学方程式为 。
(2)实验1的现象表明,猜想与假设1 (填“成立”或“不成立”)。
(3)由实验2得出结论:出现“溶液变红后褪色”现象的原因是 。
(4)实验3的操作步骤:取3支试管,分别加入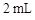 水, 。
水, 。
【反思与评价】
(5)依据现有实验,为了确保红色不变,若酚酞溶液浓度为 ,建议选用NaOH溶液的浓度
,建议选用NaOH溶液的浓度
为 %。
(6)有同学认为,仅通过实验3得出“猜想与假设Ⅲ成立”证据不足,理由是 。
【2015年福建省泉州市】为提高实验探究能力,某化学兴趣小组的同学在老师的指导下,对一瓶久置出现变质硬化的氢氧化钙固体进行如下探究活动。
【探究活动一】试验硬化的氢氧化钙样品是否完全变质
(1)用化学方程式表示氢氧化钙变质的原因: 。
(2)检验氢氧化钙样品是否完全变质,进行如下实验:
| 实验步骤 |
实验现象 |
实验结论 |
| 取氢氧化钙样品少量,研细后加适量蒸馏水 充分混合后静置, |
|
该样品还含有氢氧化钙 |
【探究活动二】测定样品中含有的变质固体(以下用R表示)的质量分数
取3克部分变质的氢氧化钙样品与足量的稀盐酸反应,测量生成气体的体积(气体不溶于植物油),从而计算出样品中R的质量,便可求出样品中R的质量分数。实验装置(气密性良好)如图1所示。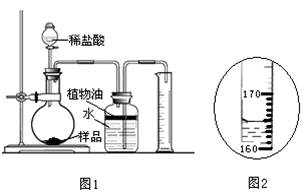
(3)将稀盐酸滴入样品中,产生气体的化学方程式为 ,反应一段时间后,当观察到 (填实验现象),才停止滴加稀盐酸。
(4)实验中量筒的作用是 。
(5)实验结束后,量筒内进入水的体积如图2所示,其读数为 mL。已知在该实验条件下,生成气体的密度为2g·L-1,通过计算,样品中R的质量分数为 。
(6)上述图1所示实验装置和相关试剂,用来实验测定样品中R的质量分数是比较粗略的,请简要说明测定数据存在误差的原因: (写一个)。