下列比较正确的是( )
| A.离子半径:Al3+>O2- | B.与水反应的激烈程度:Al>Mg |
| C.热稳定性:HF>NH3 | D.单质的氧化性:S>O2 |
设氯原子的质量为ag,12C原子的质量为bg,用NA表示阿伏加德罗常数的值,则下列说法正确的是
| A.氯元素的相对原子质量为12/b | B.mg该氯原子的物质的量为m / NA mol |
| C.该氯原子的摩尔质量是a NA | D.ng该氯原子所含的电子数是17n/a |
同温同压下,对于等体积的一氧化氮(14N18O)和一氧化碳(13C18O)气体,下列说法正确的是:
| A.含相同的分子数和原子数 | B.含相同的分子数和电子数 |
| C.含相同的质子和中子数 | D.所含分子数和质量均不相同 |
两种微粒的质子数和电子数都相等,它们不可能是
| A.一种阳离子和一种阴离子 | B.一种原子和一种分子 |
| C.一种单质分子和一种化合物分子 | D.一种分子和一种离子 |
下列反应的离子方程式书写正确的是
A.向NH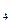 HSO HSO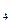 稀溶液中逐滴加入Ba(OH) 稀溶液中逐滴加入Ba(OH) 稀溶液至刚好沉淀完全: 稀溶液至刚好沉淀完全:Ba  +2OH +2OH +NH +NH +H +H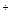 +SO +SO ====BaSO ====BaSO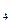 ↓+NH ↓+NH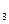 ·H ·H O+H O+H O O |
| B.将标准状况下112mL氯气通入10mL浓度为1mol/L的溴化亚铁溶液中: 2Fe2+ + 4Br- +3Cl2 ="==" 2Fe2+ + 6Cl- +2Br2 |
C.向硅酸钠溶液中通入过量的CO :SiO :SiO +CO +CO +H +H O====H O====H SiO SiO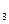 ↓+CO ↓+CO |
| D.硫酸亚铁溶液中加过氧化氢溶液:Fe2+ + 2H2O2 + 4H+ = Fe3+ + 4H2O |
阿伏加德罗常数约为6.02×1023mol-1,下列叙述中正确的是
⑴.0.25molNa2O2中含有的阴离子数为0.5×6.02×1023⑵.7.5gSiO2晶体中含有的硅氧键数为0.5×6.02×1023⑶.2.24LCH4中含有的原子数为0.5×6.02×1023
⑷.250mL2mol/L的氨水中含有NH3·H2O的分子数为0.5×6.02×1023⑸.1L 1mol·L―1的HAc溶液中含有6.02×1023个氢离子⑹.18g D2O(重水)完全电解,转移
6.02×1023个电子⑺.22.4L SO2气体,所含氧原子数为2×6.02×1023
⑻.14g乙烯和丙烯的混合物中,含有共用电子对数目为3×6.02×1023
| A.2个 | B.3个 | C.5个 | D.6个 |