下列说法错误的是
| A.含有离子键的化合物一定是离子化合物 |
| B.在共价化合物中一定含有共价键 |
| C.含有共价键的化合物一定是共价化合物 |
| D.双原子单质分子中的共价健一定是非极性键 |
下列离子方程式正确的是( )
A.二氧化硫通入足量KOH溶液中SO2+2OH-  +H2O +H2O |
B.往澄清石灰水中通入足量二氧化硫SO2+Ca2++2OH- CaSO3↓+H2O CaSO3↓+H2O |
C.往二氧化硫的水溶液中滴加少量NaOH溶液H2SO3+OH-  +H2O +H2O |
D.亚硫酸中滴加双氧水生成硫酸H2SO3+2H++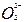  2H++ 2H++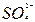 +2H2O +2H2O |
在氯化钡溶液通入SO2,溶液仍澄清,若将氯化钡溶液分装两支试管,一支加硝酸,另一支加NaOH溶液,然后再通入SO2,结果两试管中都有白色沉淀生成,由此得出下列结论合理的是( )
| A.氯化钡有两性 |
| B.两支试管中的白色沉淀都是BaSO4 |
| C.SO2具有还原性和酸性 |
D.加碱后溶液中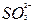 浓度增大 浓度增大 |
为了除去SO2中的SO3,以制得纯的SO2,下列试剂最好选用( )
| A.石灰水 | B.饱和NaHSO3 |
| C.浓H2SO4(98.3%) | D.饱和Na2SO3溶液 |
下列实验能证明有SO2存在的是( )
①能使澄清石灰水变浑浊②能使湿润的蓝色石蕊试纸变红③能使品红溶液褪色④通入足量的NaOH溶液中再滴加BaCl2溶液有白色沉淀生成,该沉淀溶于稀盐酸⑤通入溴水中能使溴水褪色,再滴加Ba(NO3)2溶液有白色沉淀生成
| A.都能证明 | B.只有⑤能证明 |
| C.③④⑤能证明 | D.都不能证明 |
往某盐溶液中加入过量的氯水,再滴入Ba(NO3)2溶液和稀硝酸,若有白色沉淀生成,则原溶液可能是( )
| A.碳酸钠溶液 | B.氯化钙溶液 |
| C.亚硫酸钠溶液 | D.Na2S |