在密闭容器中加入等浓度的CO与H2O,T ℃时发生如下反应:
CO(g)+H2O(g)  CO2(g)+H2(g) ΔH< 0
CO2(g)+H2(g) ΔH< 0
已知CO的浓度变化如图所示,第4 minCO的浓度不再改变。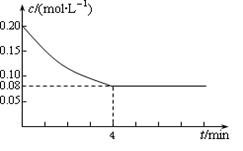
(1)从0~4 min,该反应的平均速率v(CO)= mol/(L·min);该反应的平衡常数表达式为:K= ;可计算得该反应的平衡常数结果为:K= 。
(2)为了增大CO的转化率,可以采取的措施有 。
| A.增大反应物中CO的浓度 |
| B.降低反应温度 |
| C.将密闭容器体积压缩至一半 |
| D.加入适宜的催化剂 |
(3)若不改变反应温度和反应物中CO的起始浓度,使CO的转化率达到90%,则水蒸气的起始浓度至少为 mol/L?
在密闭容器中加入NaHCO3和NaOH的混合物共36.8 g,加热至250℃,经充分反应后排出气体,冷却得到剩余固体质量为33.2 g,试计算原固体混合物中两种组分的质量(写出必要的计算过程)。
有NH4+、Fe3+、NO3-、Fe2+、H+ 和H2O六种微粒,分别属于一个氧化还原反应中的反应物和生成物。
(1).氧化剂与还原剂的物质的量之比为
(2).若有l mol NO3-参加反应,则转移mol e-
(3).若把该反应设计为原电池,则负极反应为
由Zn—Cu—H2SO4组成的原电池,工作一段时间后,锌片的质量减少了6.5g。求:
(1)原电池的_______极生成氢气_______L(标准状况)。
(2)已知:1mol氢气完全燃烧放出285.8kJ的热量。将(1)中获得的氢气燃烧,可以得到_________kJ的热量。
(3)若将电解质溶液改为硫酸铜溶液,当电池输出相同的电量时,电池两极的质量差为_____________。
在标准状况下,2.24L的某气态烷烃和具有一个双键的烯烃的混合气体完全燃烧后,将高温下产生的气体缓慢通过浓硫酸,浓硫酸增重4.05g,剩余气体通过碱石灰,碱石灰增重6.60g。
问:(1)混合气体由哪两种烃组成,写出它们的结构简式。
(2)混合气体中两种烃的体积分数各为多少?
为了测定某铜银合金的成分。将30.0g合金完全溶于80ml 13.5mol/L的浓HNO3中,待合金完全溶解后,收集到NO和NO2的混合气体共6.72L(标准状况),并测得溶液中氢离子浓度为1mol/L。假设反应后溶液的体积仍为80ml。试计算:
(1)被还原的硝酸的物质的量。
(2)合金中银的质量分数。