已知乙炔与苯蒸汽完全燃烧的热化学方程式如下所示:
①C2H2(g)+5/2O2(g)→2CO2(g)+H2O(1) △H=-1300KJ/mol
②C6H6(g)+15/2O2(g)→6CO2(g)+3H2O(1)△H=-3295Kj/mol
下列说法正确的是 ( )
| A.1mol C2H2(g)完全燃烧生成气态水时放热大于1300kJ |
| B.1mol C6H6(1)完全燃烧生成液态水时放热大于3295kJ |
| C.相同条件下,等质量的C2H2(g)与C6H6(g)完全燃烧,C6H6(g)放热更多 |
| D.C2H2(g)三聚生成C6H6(g)的过程属于放热反应 |
向60 mL Na2SO4溶液中加入BaCl2溶液,有关数据见下表:
下列有关说法不正确的是
| A.混合前,BaCl2溶液的物质的量浓度为0.10 mol·L-1 |
| B.混合前,Na2SO4溶液的物质的量浓度为0.15 mol·L-1 |
| C.3号实验中沉淀的质量x为1.398 g |
| D.完全沉淀60 mL Na2SO4溶液消耗BaCl2溶液的体积为80 mL |
我国知名企业比亚迪公司开发了具有多项专利的锂钒氧化物二次电池,其成本较低,对环境无污染,能量密度远远高于其他材料电池,电池总反应为V2O5+xLi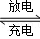 LixV2O5.下列说法中正确的是
LixV2O5.下列说法中正确的是
| A.电池在放电时,Li+向负极移动 |
| B.锂在放电时做正极,充电时为阳极 |
| C.该电池充电时阳极的反应为LixV2O5﹣xe﹣═V2O5+xLi+ |
| D.V2O5只是锂发生反应的载体,不参与电池反应 |
下列图中的实验方案,能达到实验目的的是
已知下列实验事实:
①Cr2O3固体既能溶于KOH溶液得到KCrO2溶液,又能溶于硫酸得到Cr2(SO4)3溶液;
②向KCrO2溶液中滴加H2O2溶液,再酸化,可得K2Cr2O7溶液;
③将K2Cr2O7溶液滴加到淀粉和KI的混合溶液中,溶液变蓝。
下列判断不正确的是
| A.化合物KCrO2中Cr元素为+3价 |
| B.实验①证明Cr2O3是两性氧化物 |
| C.实验②证明H2O2既有氧化性又有还原性 |
| D.实验③证明氧化性:Cr2O72- > I2 |
A、B、C、D是原子序数依次增大的四种短周期元素,甲、乙、丙、丁、戊是由其中的两种或三种元素组成的化合物,辛是由C元素形成的单质。已知反应:甲+乙=丁+辛,甲+丙=戊+辛;常温下0.1 mol/L 丁溶液的pH为13。下列说法正确的是
A.元素B在周期表中的位置为第二周期第VIA族
B.元素B、C、D的原子半径由大到小的顺序为r(D)>r(C)>r(B)
C.1.0 L、0.1 mol/L戊溶液中阴离子总的物质的量小于0.1 mol
D.1 mol甲与足量的乙完全反应共转移了约6.02×1023个电子