我国知名企业比亚迪公司开发了具有多项专利的锂钒氧化物二次电池,其成本较低,对环境无污染,能量密度远远高于其他材料电池,电池总反应为V2O5+xLi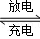 LixV2O5.下列说法中正确的是
LixV2O5.下列说法中正确的是
| A.电池在放电时,Li+向负极移动 |
| B.锂在放电时做正极,充电时为阳极 |
| C.该电池充电时阳极的反应为LixV2O5﹣xe﹣═V2O5+xLi+ |
| D.V2O5只是锂发生反应的载体,不参与电池反应 |
某固体仅由一种元素组成,其密度为5.0 g·cm-3。用X射线研究该固体的结构时得知:在边长为10-7 cm的正方体中含有20个原子,则此元素的相对原子质量最接近于下列数据中的()。
| A.32 | B.120 | C.150 | D.180 |
关于金属晶体的体心立方密堆积的结构型式的叙述中,正确的是()。
| A.晶胞是六棱柱 |
| B.属于A2型密堆积 |
| C.每个晶胞中含有4个原子 |
| D.每个晶胞中含有5个原子 |
要使金属晶体熔化必须破坏其中的金属键。金属晶体熔、沸点高低和硬度大小一般取决于金属键的强弱,而金属键的强弱与金属阳离子所带电荷的多少及半径大小相关。由此判断下列说法正确的是()。
| A.金属镁的硬度大于金属铝 |
| B.碱金属单质的熔、沸点从Li到Cs是逐渐增大的 |
| C.金属镁的熔点大于金属钠 |
| D.金属镁的硬度小于金属钙 |
下列有关金属键的叙述错误的是()。
| A.金属键没有饱和性和方向性 |
| B.金属键是金属阳离子和自由电子之间存在的强烈的静电吸引作用 |
| C.金属键中的电子属于整块金属 |
| D.金属的性质和金属固体的形成都与金属键有关 |
如图是CsCl晶体的晶胞结构(晶体中最小重复单元),已知晶体中两个最近的Cs+核间距离为a cm,氯化铯的式量为M,NA为阿伏加德罗常数,则氯化铯晶体的密度为()。
A. g·cm-3 g·cm-3 |
B.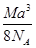 g·cm-3 g·cm-3 |
C.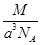 g·cm-3 g·cm-3 |
D. g·cm-3 g·cm-3 |