价电子排布式为2s22p5的原子,下列有关它的描述正确的是( )
| A.原子序数为7 | B.第一电离能最大 | C.原子半径最大 | D.电负性最大 |
下列关于硝酸参加反应的化学方程式或离子方程式书写正确的是 ( )
| A.常温下,将铁片置于浓硝酸中:Fe+6HNO3====Fe(NO3)3+3NO2↑+3H2O |
| B.Fe3O4与稀硝酸反应:Fe3O4+8H+====Fe2++2Fe3++4H2O |
C.向硝酸亚铁溶液中加入稀盐酸:3Fe2++2H++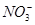 ====3Fe3++NO↑+H2O ====3Fe3++NO↑+H2O |
D.向浓硝酸中加入铜片:Cu+4H++2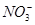 ====Cu2++2NO2↑+2H2O ====Cu2++2NO2↑+2H2O |
工业制硝酸和工业制硫酸的设备中,相同的是 ( )
| A.接触室 | B.沸腾炉 | C.吸收塔 | D.转化器 |
现有下列物质:①氯水;②氨水;③浓硝酸;④氢氧化钠;⑤溴。实验室中常保存在棕色瓶里的是( )
| A.全部 | B.①②③⑤ | C.①②④ | D.只有①③ |
下列关于浓硝酸、浓硫酸和浓盐酸的叙述中,正确的是
| A.常温下都可以用铁器或铝器贮存 |
| B.露置在空气中,容器内酸液的质量都减轻 |
| C.常温下都能与铜较快反应 |
| D.露置在空气中,容器内酸液的浓度都降低 |
近年来,冠以“绿色”的新概念不断产生,如绿色食品、绿色材料、绿色能源、绿色化学等,这里的“绿色”是对人类社会可持续发展战略的形象表述。“绿色化学”要求从经济、环保和技术上设计可行的化学反应。据此,由单质镁制硝酸镁的下列四个方案中,你认为可行而且符合“绿色化学”要求的方案是 ( )
A.Mg Mg(NO3)2 Mg(NO3)2 |
B.Mg MgCl2 MgCl2 Mg(OH)2 Mg(OH)2 Mg(NO3)2 Mg(NO3)2 |
C.Mg MgO MgO Mg(NO3)2 Mg(NO3)2 |
D.Mg MgSO4 MgSO4 Mg(NO3)2 Mg(NO3)2 |