俗话说, “陈酒老醋特别香”,其原因是酒在储存过程中生成了有香味的乙酸乙酯,在实验室里我们也可以用如图所示的装置来模拟该过程。请回答下列问题:
(1)在大试管中需加入浓硫酸、冰醋酸各2mL,乙醇3mL,加入试剂的正确的操作是 。
(2)浓硫酸的作用是:① ;② 。
(3)饱和碳酸钠溶液的主要作用是 。
(4)装置中通蒸气的导管只能插到饱和碳酸钠溶液的液面处,不能插入溶液中,目的 ,长导管的作用是 。
(5)若要把制得的乙酸乙酯分离出来,应采用的实验操作是 。
(6)进行该实验时,最好向试管甲中加入几块碎瓷片,其目的是 。
(7)试管乙中观察到的现象是____________________,由此可见,乙酸乙酯的密度比水________(填“大”或“小”),而且______。
(8)生成乙酸乙酯的反应是可逆反应,反应物不能完全转化为生成物,反应一段时间后,就达到了该反应的限度,即达到化学平衡状态。下列描述能说明该反应已达到化学平衡状态的是(填序号) 。
①单位时间里,生成1mol乙酸乙酯,同时生成1mol水
②单位时间里,生成1mol乙酸乙酯,同时生成1mol乙酸
③单位时间里,消耗1mol乙醇,同时消耗1mol乙酸
④正反应的速率与逆反应的速率相等
⑤混合物中各物质的浓度不再变化
现拟用下图所示装置(尾气处理部分略)来制取一氧化碳,并用以测定某铜粉样品(混有CuO粉末)中金属铜的含量。
|
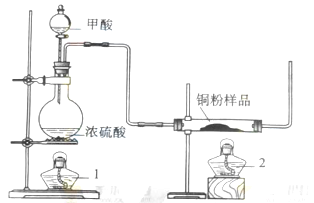 .
.
(16分)某同学利用下列装置实现铜与浓硝酸、稀硝酸反应,过程如下:
I.取一段铜丝,用稀硫酸除去铜锈[主要成分是Cu2(OH)2CO3]。
Ⅱ.将洗涤后的铜丝做成匝数较多的螺旋状。
III.按如图所示装置连接仪器、检查气密性、装入化学试剂。
(1)过程I发生反应的离子方程式是。
(2)写出过程III中检查气密性的方法。
⑶过程III的后续操作如下:
①打开止水夹a和b,轻推注射器,使浓硝酸与铜丝接触,观察到的现象是,一段时间后使反应停止的操作是,关闭a,取下注射器。
②打开b和分液漏斗活塞,当玻璃管充满稀硝酸后,关闭b和分液漏斗活塞,打开a,观察到有气泡产生。稀硝酸充满玻璃管的实验目是,该反应的离子方程式是。
(4)另取3支盛满NO2气体的小试管分别倒置在盛有常温水、热水和冰水的3只烧杯中,发现液面上升的高度明显不一致。结果如下表所示(忽略温度对气体体积的影响):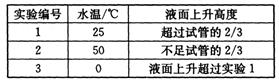
①根据上表得出的结论是温度越(填“高”或“低”),进入试管中的溶液越多。
②查阅资料:
a.NO2与水反应的实际过程为:2NO2+H2O=HNO3+HNO23HNO2 =HNO3+2NO+H2O;
b.HNO2不稳定。
则产生上述现象的原因是。
在实验室里可用右图所示装置制取氯酸钾、次氯酸钠和探究氯水的性质。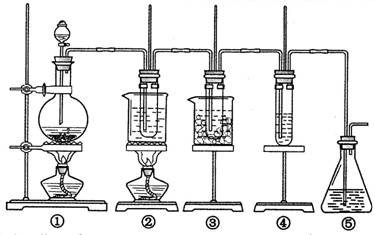
图中:①为氯气发生装置;②的试管里盛有15 mL 30% KOH溶液,并置于热水浴中;③的试管里盛有15 mL 8% NaOH溶液,并置于冰水浴中;④的试管里加有紫色石蕊试液;⑤为尾气吸收装置。请填写下列空白:
(1)装置①是氯气发生装置,蒸馏烧瓶中盛放MnO2固体,其反应的化学方程式为。
(2)如果实验室中MnO2用完了,则下列物质可能可以用来代替MnO2制Cl2的是:
A.NaBiO3 B.FeCl3 C.PbO2
已知氧化性强弱顺序为:NaBiO3>PbO2>MnO2>FeCl3
(3)比较制取氯酸钾和次氯酸钠的条件,二者的差异是
①;②。
(4)反应完毕经冷却后,②的试管中有大量晶体析出。右图中符合该晶体溶解度曲线的是(填写编号字母);从②的试管中分离出该晶体的方法是(填写实验操作名称)。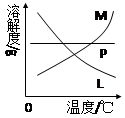
(5)根据④的试管里紫色石蕊试液的颜色变化可否证明氯气的强氧化性。为什么?。
(6)一定量的氢气在氯气中燃烧,所得的混合物用100mL 3.00mol/L的NaOH溶液(密度为1.2g/mL)恰好完全吸收,测得溶液中含有NaClO的物质的量为0.0500mol。所得溶液中Cl-离子的物质的量。
实验室欲配制250mL 0.2 mol·L-1的碳酸钠溶液,回答下列问题:
可供选择的仪器:①量筒②胶头滴管③托盘天平④药匙⑤烧瓶⑥烧杯
(1)通过计算可知,应用托盘天平称取g碳酸钠晶体(Na2CO3•10H2O)。
(2)配制过程需要的仪器_____________(填序号),还缺少的仪器有。
(3)配制时,正确的操作顺序是(用字母表示,每个字母只能用一次)_____________;
| A.用30mL水洗涤烧杯2~3次,洗涤液均注入容量瓶 |
| B.用托盘天平准确称取所需的Na2CO3•10H2O晶体的质量,放入烧杯中,再加入少量水(约30mL),用玻璃棒慢慢搅动,使其充分溶解 |
| C.将已冷却的溶液沿玻璃棒注入250mL的容量瓶中 |
| D.将容量瓶盖紧,振荡,摇匀 |
E.改用胶头滴管加水,使溶液凹液面恰好与刻度相切
F.继续往容量瓶内小心加水,直到液面接近刻度1~2cm处
(4)若出现如下情况,对所配溶液浓度将有何影响(填“偏高”、“偏低”或“无影响”)。若没有进行A操作______________;若定容时俯视刻度线_______________。
实验室用下列仪器组装一套蒸馏石油的装置,并进行蒸馏得到汽油和煤油。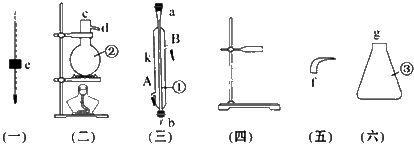
(1)写出下列仪器的名称:
①__________________;②___________________;③_________________。
(2)将以上仪器按从左到右顺序,用字母a、b、c……进行连接:
e接();()接();()接()接()
(3)①仪器的A口是__________,B口是__________。
(4)蒸馏时,温度计水银球应在______________________(位置)。
(5)在②中注入原油后,加几片碎瓷片的目的是_________________。