下列有关化学用语使用正确的是:
A.硫离子的结构示意图: |
B.NH4Cl的电子式: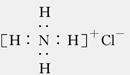 |
| C.原子核内有10个中子的氧原子:18 8O | D.Na2O2的电子式为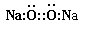 |
中华商务网讯:2011年中国将超北美成为全球液晶显示器第二大市场。生产液晶显示器的过程中使用的化学清洗剂NF3是一种温室气体,其存储能量的能力是CO2的12000~20000倍,在大气中的寿命可长达740年,以下是几种化学键的键能:
| 化学键 |
N≡N |
F—F |
N—F |
| 键能/(kJ·mol-1) |
941.7 |
154.8 |
283.0 |
下列说法中正确的是 ( )
A.过程N2(g)→2N(g)放出能量
B.过程N(g)+3F(g)→NF3(g)放出能量
C.反应N2(g)+3F2(g)→2NF3(g)的ΔH>0
D.NF3吸收能量后如果没有化学键的断裂与生成,仍可能发生化学反应
固体A的化学式为NH5,它的所有原子的最外层电子结构都符合相应稀有气体原子的最外层电子结构,则下列有关说法中不正确的是 ( )
| A.NH5中既有离子键又有共价键 |
| B.NH5的熔沸点高于NH3 |
| C.1 mol NH5中含有5 mol N—H键 |
| D.将固体A投入少量水中,可生成H2和NH3·H2O |
下表为元素周期表前四周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中,正确的是 ( )
| A.常压下五种元素的单质中W单质的沸点最高 |
| B.Z元素的最高价氧化物对应的水化物酸性最强 |
| C.X的氢化物比同族元素的氢化物沸点低 |
| D.Y、Z和W的阴离子半径依次增大 |
X、Y、Z为短周期元素,原子序数依次增大。X的最外层电子数是Y原子最外层电子数的2倍,质子数比Y少5,X、Z在同主族。下列叙述不正确的是( )
| A.原子半径:Y>Z |
| B.X元素的一种单质可用于消毒杀菌 |
| C.Y的氧化物是工业制取Y单质的主要原料 |
| D.Z的单质在氧气中点燃可生成两种酸性氧化物 |
下列有关物质性质的比较正确的是( )
①同主族元素的单质从上到下,非金属性减弱,熔点增高 ②所有元素的最高正化合价在数值上等于它所在的族序数
③同周期主族元素的原子半径越小,越难失去电子 ④元素的非金属性越强,它的气态氢化物水溶液的酸性越强 ⑤酸性:HClO4>H2SO4>H3PO4>H2SiO3
| A.①③ | B.②④ | C.③⑤ | D.②⑤ |