某兴趣小组的同学用下图所示装置研究有关电化学的问题(甲、乙、丙三池中溶质足量),当闭合该装置的电键K时,观察到电流计的指针发生了偏转。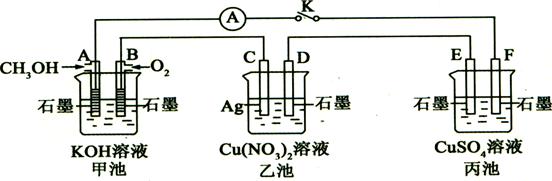
请回答下列问题:
(1)甲池为 (填“原电池”、“电解池”或“电镀池”),
A电极的电极反应式为 。
(2)丙池中F电极为 (填“正极”、“负极”、“阴极”或“阳极”),该池的总反应方程式为 。
(3)当乙池中C极质量减轻5.4g时,甲池中B电极理论上消耗O2的体积为 ml(标准状况)。
(4)一段时间后,断开电键K。下列物质能使乙池恢复到反应前浓度的是 (填选项字母)。
| A.Cu | B.CuO | C.Cu(OH)2 | D.Cu2(0H)2CO3 |
目前,汽车尾气已成为许多大城市空气的主要污染。汽车尾气中含 有CO、NO等多种污染物。
(1)汽车燃料中一般不含氮,尾气中所含的NO 产生的原因是 ,化学方程式为 。
(2)治理汽车尾气中NO和CO的一种方法是:在汽车的排气管上装上一个催 化转化装置,使NO 和 CO反应,生成CO2和N2。反应的化学方程式为 。
(3)下列措施中,能减少或控制汽车尾气污染有效且可行的是 。
① 制定严格的尾气排放标准,并严格执行。
② 开发清洁能源,如氢能汽车、 太阳能汽车等。
③ 市民出行带防毒面具。
④ 市民大量移居城市郊区。
通常用饱和NaHCO3溶液除去混在CO2中的少量HCl气体,其反应的离子方程式为 ;不能用NaOH溶液的原因是 (用离子方程式表示);也不能用 Na2CO3溶液吸收的原因是 (用离子方程式表示)。
根据下图中A、B两种固体物质的溶解度曲线,回答下列问题:
(1)10oC时,将10gB溶于100g水中,形成溶液的质量是 ,将它变成饱和溶液可采用的一种方法是 。
(2)P点的含义是 。在30oC时,A、B两物质饱和溶液的溶质质量分数的大小关系为A B(填“>”“<”或“=”)。当A中含有少量B 时,提纯A所采用的方法为 。
人类的衣、食、住、行都离不开化学,请结合化学知识回答下列问题。
(1)为了美观耐磨且不易褪色,我们所穿的校服都要加入一定比例的聚酯纤维,它属于 材料。
(2)为了身体健康,我们每天食用很多蔬菜和水果,其中富含的营养素是 。
(3)我们常用洗涤剂清洗餐具上的油污,这是因为洗涤剂具有 功能。
(4)为了倡导低碳生活,我选择每天骑自行车上下学。但自行车很容易淋雨生锈,应采取的防锈措施是 ,原理 。
用化学符号填空
氮元素 两个氢离子 氧分子
五氧化二磷中磷元素的化合价