(1)现有可逆反应:aA(g)+ bB(g) cC(g)+ dD(g);根据下图示回答:
cC(g)+ dD(g);根据下图示回答:
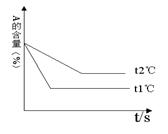
①上左图中压强 p1 p2(填“>”、“<”、“=”)
②反应式中(a +b) (c +d)(填“>”、“<”、“=”)
③上右图中温度t1℃ t2℃(填“高”或“低”)
④该反应的正反应为 反应(填“吸热”或“放热”)
(2)今有①CH3COOH;②HCl;③H2SO4三种溶液,选择填空:
| A.①>②>③ | B.①<②<③ | C.①=②=③ E.①>②=③ |
| D.①=③>② F.①<②=③ G.①=②<③H.①=②>③ |
①当它们pH相同时,其物质的量浓度关系是 。
②当它们的物质的量浓度相同时,其pH的关系是 。
③中和等体积、等物质的量浓度的三种酸溶液,需同物质的量浓度的烧碱溶液的体积关系为 。
④当它们pH相同、体积相同时,同时加入锌,则开始时反应速率大小关系为 。
⑤将pH相同的三种酸均稀释10倍后,pH关系为
⑥当它们pH相同、体积相同时,同时加入足量的锌,最终收集到的氢气的体积关系为 。
(15分)铁及其化合物在国民经济、日常生活中占有非常 重要的地位,了解铁及其化合物的性质和用途非常重要。请回答下列问题:
重要的地位,了解铁及其化合物的性质和用途非常重要。请回答下列问题:
(1)铁在自然界中以态存在,其氧化物呈黑色的是,呈红褐色的是(填写化学式)。
(2)铁在纯氧气中燃烧的化学方程式为。
铁在氯气中反应的产物是。
(3)要验证一种溶液中是否含有Fe3+、Fe2+,正确的实验方法是。
A.向甲试管中 加入试液,滴入KSCN溶液,若显血红色,证明一定存在Fe3+。
加入试液,滴入KSCN溶液,若显血红色,证明一定存在Fe3+。
B.向乙试管中加入试液,滴入氯水,若氯水褪色,证明一定存在Fe2+。
C.向丙试管中加入试液,滴入氯水,再滴入KSCN溶液,若显血红色,证明原溶液中一定存在Fe3+
(4)铁合金有下列数据:
| 钢 |
|||
| 碳素钢(Fe、C、Mn、Si) |
合金钢 |
||
| 低碳钢 |
中碳钢 |
高碳钢 |
碳素钢+Cr、Mn、W、Ni、Co等 |
| 含碳量<0.3% |
含碳量0.3%--0.6% |
含碳量>0.6% |
|
| 韧性好,强度低 |
韧性好、强度好 |
硬而脆 |
具有特殊性能 |
取15g某碳素钢样品,按下列实验流程进行操作:
①A、B的作用是,
②充分加热完全反应后,D装置质量增加0.022g,该样品属于钢。
③没有A、B装置,实验结果(填“偏高”“偏低”“不影响”)
(16分)硫及其化合物有如下转化关系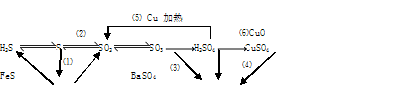
(1)发生氧化还原反应的是(填序号)
(2)写出(5)的反应方程式,
说明浓硫酸具有,制取CuSO4,方法最好(填序号),
(3)SO2是造成空气污染,形成酸雨的主要物质。SO2在水的存在下与氧气反应生成硫酸,反应方程式为。
验证二氧化硫的方法是。
(4)某溶液中含有Cl-、SO42-,可能含有Na+、Fe2+或其中一种。
①验证Cl-、SO42-的方法是
A.先加BaCl2溶液,等沉淀后,再加AgNO3溶液
B.先加AgNO3溶液,等沉淀后,再加BaCl2溶液
C.先加Ba(NO3)2溶液,等沉淀后,再加AgNO3溶液
②验证Na+或Fe2+最简单的方法是。
(12分)实验室制取Cl2及性质的验证实验组合装置如下:
A B C D E F G
回答下列问题:
(1)A中的化学方程式为。
(2)B的作用是除去HCl气体,C的作用是。
(3)E、F中观察到的现象分别是,你得到的结论是。
(4)G的作用是,
化学方程式为。
(14分)家庭厨房中的:
| A.食盐 | B.食醋 | C.淀粉 | D.油脂 E.蛋白质 F.果汁,请按下列要求填空(填序号) |
(1)人类的生命活动需要、糖类、、
水和无机盐等六类营养物质。
(2)含丰富维生素C的是,维生素又称,在人体内有重要功能。
(3)经过水解可直接进入血液,补充能量的是。
(4)既可作为中性调味品,又可作防腐剂的是。
(5)食用过多的会引起血压升高、肾脏受损。
,(1)以甲烷为燃料制作新型燃料电池,电解质为氢氧化钾溶液。电池负反应式为;放电时钾离子移向电池的(填“正”或“负”)极
(2)碳氢化合物完全燃烧生成CO2和H2O。常温常压下,空气中的CO2溶于水,达到平衡时,溶液pH=5.60,c(H2CO3)=1.5×10-5 mol·L-1。若忽略水的电离及H2CO3的第二级电离,
则H2CO3  HCO3-+H+的平衡常数K1=(已知10-5.60=2.5×10-6)
HCO3-+H+的平衡常数K1=(已知10-5.60=2.5×10-6)
(3)常温下,0.1 mol·L-1NaHCO3溶液的pH大于8,则溶液中
c(H2CO3)c(CO32-)(填“>”、“=”或“<”),原因是
(用离子方程式和必要的文字说明)。