下表为部分短周期元素的原子半径及主要化合价,根据表中信息判断,下列叙述正确的是
| 元素代号 |
X |
Y |
Z |
M |
N |
| 原子半径/nm |
0.160 |
0.143 |
0.102 |
0.071 |
0.099 |
| 主要化合价 |
+2 |
+3 |
+6、-2 |
-1 |
-1 |
A.X、Y最高价氧化物对应水化物的碱性:Y>X
B.最高价氧化物对应的水化物的酸性: H2ZO4>HNO4
C.气态氢化物的稳定性:HM<H2Z
D.M、N形成的简单离子的还原性:N->M-
在元素周期表中短周期的X和Y两种元素可组成化合物XY3,则下列说法正确的是
| A.XY3晶体一定是分子晶体 |
| B.XY3中各原子的最外层一定满足8电子的稳定结构 |
| C.X和Y一定不属于同一主族 |
| D.Y原子序数为m,X原子序数可能是m±4或m+6 或m+8等 |
下列物质进行一氯取代反应后,生成4种沸点不同的有机产物的是
| A.2,2-二甲基丁烷 | B.2,2-二甲基-3-乙基戊烷 |
| C.2,3-二甲基戊烷 | D.2,2,3-三甲基戊烷 |
某离子晶体中晶体结构最小的重复单元如图:A为阴离子,在正方体内,B为阳离子,分别在顶点和面心,则该晶体的化学式为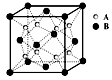
| A.B2A | B.BA2 | C.B7A4 | D.B4A7 |
现有部分短周期元素的性质或原子结构如下表:
| 元素编号 |
元素性质或原子结构 |
| T |
最外层电子数是次外层电子数的2倍 |
| X |
L层有三个未成对电子 |
| Y |
L层p电子数比s电子数多两个 |
| Z |
元素的最高正价为+7价 |
下列说法正确的是
A.Z离子的结构示意图为: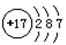 |
B.分子TY2的键角为180° |
C.T元素在周期表中的表示为: |
D.XZ3为非极性分子 |
下列说法正确的是
| A.乙硫醇(CH3CH2-SH)比乙醇(CH3CH2-OH)熔点低原因是乙醇分子间易形成氢键 |
| B.氯化钠易溶于水是因为形成了氢键 |
| C.氨易液化与氨分子间存在氢键无关 |
| D.H2O是一种非常稳定的化合物,这是由于氢键所致 |