1,2-二溴乙烷可作汽油抗爆剂的添加剂,常温下它是无色液体,密度是2.18 g/cm3,沸点131.4℃,熔点9.79℃,不溶于水,易溶于醇、醚、丙酮等有机溶剂。在实验中可以用下图所示装置制备1,2-二溴乙烷。其中分液漏斗和烧瓶a中装有乙醇和浓硫酸的混合液,试管d中装有浓溴水(表面覆盖少量水)。请填写下列空白:
(1)烧瓶a中发生的是乙醇的脱水反应,即消去反应,反应温度是170℃,并且该反应要求温度迅速升高到170℃,否则容易发生副反应。请写出乙醇发生消去反应的方程式 。
(2)写出制备1,2-二溴乙烷的化学方程式: 。
(3)安全瓶b可以防止倒吸,并可以检查实验进行时试管d是否发生堵塞。请回答发生堵塞时瓶b中的现象: 。
(4)容器c中NaOH溶液的作用是: 。
(5)某学生做此实验时,使用一定量的液溴,当溴全部褪色时,所消耗乙醇和浓硫酸混合液的量比正常情况下超出许多,如果装置的气密性没有问题,试分析其可能的原因_______________。
A、B、C、D、E、F为短周期主族元素,原子序数依次增大,A原子中不含中子; C、D同周期;D的质子数 比B与C的最外层电子数之和少1,D的最外层电子数是次外层电子数的3倍;E与A同族,F与E同周期并且是该周期原子半径最小的金属元素。
⑴由A、B元素组成的是石油化工生产标志的物质的结构式是:
⑵由A、D、E元素组成的物质与A、D、F元素组成的物质反应的离子方程式是:__________
⑶B、C、D分别与A组成最简单化合物的稳定性从大到小顺序是:
⑷由A、C、D元素组成盐含有的化学键有(填化学键类型)该物质与A、D、E元素组成的物质反应的方程式是:
⑸E、F所在的金属元素最高价氧化物对应水化物的碱性由弱到强顺序是(用化学式表示)
(1)为了降低汽车尾气对大气的污染,有关部门拟用甲醇替代液化石油气作为公交车的燃料。已知:在25℃10kPa下,10g甲醇燃烧生成CO2和液态水时放热226.8kJ。请写出表示甲醇燃烧的热化学方程式:
(2)某些化学反应可用下式表示:A + B  C + D + H2O
C + D + H2O
请回答下列问题:
①若A、D均可用于消毒,且C是家家户户的厨房必备的调味品之一,写出该反应的离子方程式。
②若A为水垢的主要成分之一,B是日常生活常见有机物(厨房用品),
写出该反应的化学方程式:。
③若C、D均为气体且都能使澄清石灰水变浑浊,则只用
或(任写两种试剂的名称)就可以鉴别C、D两种气体。
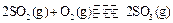 反应过程的能量变化如图所示。已知
反应过程的能量变化如图所示。已知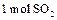 氧化为
氧化为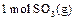 的
的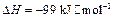 。请回答问题:
。请回答问题:
(1)图中A、C分别表示、,E的大小对该反应的
反应热有无影响?。该反应通常用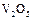 作催化剂,加
作催化剂,加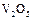 会使图中
会使图中
B点升高还是降低?,理由是 。
(2)图中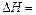
 。
。
(3)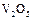 的催化循环机理可能为:
的催化循环机理可能为: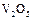 氧化
氧化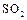 时,自身被还原为四价钒化合物;四价钒化合物再被氧气氧化。写出该催化循环机理的化学方程式 。
时,自身被还原为四价钒化合物;四价钒化合物再被氧气氧化。写出该催化循环机理的化学方程式 。
(4)如果反应速率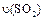 为
为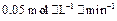 ,则
,则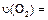
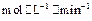 、
、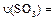
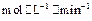 。
。
(5)已知单质硫的燃烧热为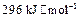 ,计算由
,计算由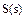 生成
生成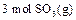 的
的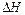 。
。
某厂的酸性工业废水中含有一定量的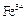 、
、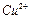 、
、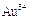 等离子。有人设计了如图所示的工艺流程,利用常用的酸、碱和工业生产中的废铁屑,从废水中回收金,并生产一定量的铁红和氧化铜。
等离子。有人设计了如图所示的工艺流程,利用常用的酸、碱和工业生产中的废铁屑,从废水中回收金,并生产一定量的铁红和氧化铜。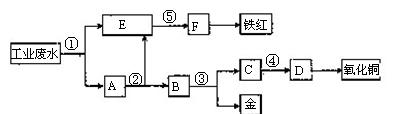
填写下面空白。
(1)图中标号处需加入的相应物质分别是①、②、③、④、⑤。
(2)写出①处发生反应的离子方程式;
写出③处发生反应的化学方程。
(3)铁红的化学式为 ;分别写出铁红和氧化铜在工业上的一种主要用途:铁红 ;氧化铜。
(1)常温下,有A、B、C、D四种无色溶液,它们分别是CH3COONa溶液、NH4Cl溶液、盐酸和NaNO3溶液中的一种。已知A、B的水溶液中水的电离程度相同,A、C溶液的pH相同。
则: B是____ __溶液(填溶质的化学式,下同),C是______,
(2)已知某溶液中只存在OH-、H+、NH4+、Cl-四种离子,某同学推测其离子浓度大小顺序有以下几种可能:
①c(Cl-)>c(NH4+)>c(H+)>c(OH-)
②c(Cl-)>c(NH4+)>c(OH-)>c(H+)
③c(NH4+)>c(Cl-)>c(OH-)>c(H+)
④c(Cl-)>c(H+)>c(NH4+)>c(OH-)
则:(ⅰ)上述关系一定不正确的是__(填序号)。
(ⅱ)若溶液中只有一种溶质,则该溶液中离子浓度的大小关系为__(填上列四种情况之一的序号);
(ⅲ)若四种离子浓度关系有c(NH4+)="" c(Cl-),则该溶液一定显__(填“酸性”、“碱性”或“中性”)。