830K时,在密闭容器中发生下列可逆反应:
CO(g)+H2O(g) CO2(g)+H2(g);△H<0 试回答下列问题:
CO2(g)+H2(g);△H<0 试回答下列问题:
(1)若起始时c(CO)="2" mol•L-1,c(H2O)="3" mol•L-1,达到平衡时CO的转化率为60%,则在该温度下,该反应的平衡常数K= .
(2)在相同温度下,若起始时c(CO)="1" mol•L-1,c(H2O)="2" mol•L-1,反应进行一段时间后,测得H2的浓度为0.5 mol•L-1,则此时该反应是否达到平衡状态 (填“是”与“否”), 此时v(正) v(逆)(填“大于”“小于”或“等于”),你判断的依据是
。
(3)若降低温度,该反应的K值将 (均填“增大”“减小”或“不变”)。
在Fe(OH)3胶体中,逐滴加入HI稀溶液,会出现一系列变化。
(1)先出现红色沉淀,原因是。
(2)随后沉淀溶解,溶液呈黄色,此反应的离子方程式是。
(3)最后溶液颜色加深,此反应的离子方程式是。
(4)若用稀盐酸代替HI稀溶液,能出现上述哪些相同的变化现象(填写上面各题序号)。
硼酸晶体成片状,有滑腻感,可作润滑剂,硼酸分子结构可表示为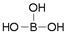 。硼酸对人体的受伤组织有缓和的防腐作用,故可用于医药和食品防腐等方面
。硼酸对人体的受伤组织有缓和的防腐作用,故可用于医药和食品防腐等方面
(1)根据以上所述可知硼酸应属于_____________。
A.强酸 B.中强酸 C.弱酸
(2)研究表明:在大多数情况下, 元素的原子在形成分子或离子时,其最外电子层具有达到8电子稳定结构的趋势。在硼酸分子中,最外层达到8个电子稳定结构的原子有_______个。
元素的原子在形成分子或离子时,其最外电子层具有达到8电子稳定结构的趋势。在硼酸分子中,最外层达到8个电子稳定结构的原子有_______个。
(3)硼酸和甲醇在浓硫酸存在的条件下,可生成挥发性硼酸三甲酯,试写出硼酸完全酯化的化学方程式(注明反应条件)_______________________________________。
(4)已知硼酸0.01mol可被20mL0.5mol·L-1NaOH溶液恰好完全中和,据此推测:硼酸在水中显酸性的原因是(写电离方程式)_________________________________。
结构化学家鲍林(Pauling)曾提出一条经验规则:设含氧酸的化学式为HnROm,其中(m-n)为非羟基氧的原子数。而含氧酸的强弱与非羟基氧原子数(m-n)有如下关系:
(m-n) 0 1 2 3
含氧酸强度弱酸中强强很强
实例 HClO H3PO4 HNO3 HClO4
请回答:
(1)按此规则判断:H3AsO4,H2SO4,HMnO4三处酸性由强到弱的顺序是_________。
(2)H3PO3和H3AsO3的分子组成相似,但酸性强弱相差很大,已知H3PO3为中强酸而H3AsO3为弱酸,试推断它们的结构式,H3PO3为__________,H3AsO3为_________。
已知在一定条件下可发生反应: ,此反应属于________反应(从分解、化合、置换、复分解反应中选择填空)。有人据此认为碘的非金属性比氯强,你认为对吗?(错对与否,都需说明原因)
,此反应属于________反应(从分解、化合、置换、复分解反应中选择填空)。有人据此认为碘的非金属性比氯强,你认为对吗?(错对与否,都需说明原因)
______________________________________________________________
以葡萄糖为燃料的微生物燃料电池的结构如图所示。
回答下列问题:
(1)该燃料电池的能量转化主要形式是;在导线中电子流动方向是(用a、b表示)。
(2)该电池负极反应式是:
。
(3)葡萄糖分子中含有的官能团是:。
该电池能否在高温下工作?理由是:
。
(4)该电池放电过程中,H+离子从(填“正”或“负”)极区向(填“正”或“负”)极区迁移。
(5)在该电池反应中,每消耗1molO2 ,理论上能生成标准状况下的
CO2L。