一种新型燃料电池,它以多孔镍板为电极插入KOH溶液中,然后分别向两极上通乙烷和氧气,其电极反应式分别为:2C2H6+36OH−–28e−=4CO32−+24H2O,14H2O+7O2+28e−=28OH−。有关此电池的叙述正确的是
| A.电解质溶液中的阴离子向正极移动 |
| B.放电一段时间后,KOH的物质的量浓度不变 |
| C.通乙烷的电极为负极 |
| D.参加反应的O2和C2H6的物质的量之比为2:7 |
下列说法正确的是
| A.装饰材料中的甲醛和芳香烃会造成居室污染 |
| B.石蜡油分解产生的气体不能使酸性高锰酸钾溶液褪色 |
| C.分子组成为CH2Cl2和C2H6O的有机物都存在同分异构现象 |
| D.油脂、葡萄糖、蛋白质都是人体重要的营养物质,它们都能发生水解反应 |
已知下表为250C时某些弱酸的电离平衡常数。下图表示常温时,稀释CH3COOH、HClO两种酸的稀溶液时,溶液pH随加水量的变化。依据所给信息,下列说法正确的是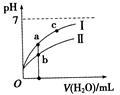
| CH3COOH |
HClO |
H2CO3 |
| Ka=1.8×10-5 |
Ka=3.0×10-8 |
Ka1=4.4×10-7Ka2=4.7×10-11 |
A.相同浓度的CH3COONa和NaClO的混合溶液中,各离子浓度的大小关系是:
C(Na+)>C(ClO—)>C(CH3COO—)>C(OH—)>C(H+)
B.向NaClO溶液中通入少量二氧化碳的离子方程式为:2ClO—+CO2+H2O═2HClO+CO32—
C.a、b、c三点所示溶液中水的电离程度c>a>b
D.图像中,Ⅰ表示CH3COOH,Ⅱ表示HClO,且溶液导电性:c>b>a
下列对有关实验事实的解释或得出的结论合理的是
| 选项 |
实验事实 |
解释或结论 |
| A |
KI淀粉溶液中滴入氯水变蓝,再通入SO2,溶液褪色 |
SO2具有漂白性 |
| B |
将BaSO4浸泡在饱和Na2CO3溶液中,部分BaSO4转化为BaCO3 |
Ksp(BaSO4)>Ksp(BaCO3) |
| C |
某钾盐溶于盐酸,产生无色无味气体,该气体通入澄清石灰水,有白色沉淀出现 |
该钾盐可能是K2CO3 |
| D |
NaI溶液 溶液变蓝色 溶液变蓝色 |
酸性条件下H2O2的氧化性比I2强 |
有机物X的蒸气相对氢气的密度为51,X中氧元素的质量分数为31.7%,则能在碱溶液中发生反应的X的同分异构体有(不考虑立体异构)
| A.15种 | B.13种 | C.11种 | D.9种 |
英国赫瑞瓦特大学陶善文博士研究出以尿素为动力的燃 料电池新技术。用这种电池可直接去除城市废水中的尿素,既能产生净化的水,又能发电。尿素燃料电池结构如图所示,关于该电池描述正确的是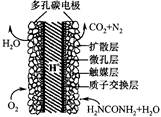
| A.电池工作时H+移向负极 |
| B.该装置还可以将电能转化成为化学能 |
| C.理论上电池工作时,每消耗67.2L O2时,可以净化2mol CO(NH2)2 |
| D.电池的负极反应式为:CO(NH2)2+H2O-6e-=CO2+N2+6H+ |