有A、B、C、D、E五种短周期元素,且相邻的A、B、C、D四种元素原子核外共有56个电子,在周期表中的位置如图所示。E的氢氧化物是两性氢氧化物, E的阳离子与A的阴离子核外电子层结构相同。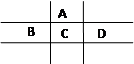
请回答下列问题:
⑴B元素在周期表中的位置为 。
⑵写出A与氢元素能形成原子物质的量之比为1∶1的化合物的电子式 ,分子中所含共价键的类型为 。
⑶比较A、C氢化物的的沸点:A C(填大于、小于或等于),
原因是 。
⑷B、C、D的原子半径由大到小的顺序为(用元素符号表示) 。
⑸若将E制作成电极与石墨用导线相连,回答下列问题:
①将两电极插入盛有稀H2SO4的烧杯中形成原电池,E电极为 极,写出该电池的总反应(用离子方程式表示) 。
②若将两电极插入盛有NaOH溶液的烧杯中,能否形成原电池?若能,请写出总反应的化学方程式 ;若不能,其理由是 。
钛铁矿的主要成分为FeTiO3(可表示为FeO·TiO2),含有少量MgO、CaO、SiO2等杂质。利用钛铁矿制备锂离子电池电极材料(钛酸锂Li4Ti5O12和磷酸亚铁锂LiFePO4)的工业流程如下图所示:
已知:FeTiO3与盐酸反应的离子方程式为:FeTiO3+4H++4Cl-=Fe2++TiOCl42-+2H2O
(1)化合物FeTiO3中铁元素的化合价是。
(2)滤渣A的成分是。
(3)滤液B中TiOCl42- 转化生成TiO2的离子方程式是。
(4)反应②中固体TiO2转化成(NH4)2Ti5O15溶液时,Ti元素的浸出率与反应温度的关系如下图所示。反应温度过高时,Ti元素浸出率下降的原因是。
(5)反应③的化学方程式是。
(6)由滤液D制备LiFePO4的过程中,所需17%双氧水与H2C2O4的质量比是。
(7)若采用钛酸锂(Li4Ti5O12)和磷酸亚铁锂(LiFePO4)作电极组成电池,其工作原理为:Li4Ti5O12+3LiFePO4 Li7Ti5O12+3FePO4
Li7Ti5O12+3FePO4
该电池充电时阳极反应式是。
铝及其化合物在生产生活中具有重要的作用。
(1)铝在元素周期表中的位置是。
(2)已知电负性的数值表示原子对电子吸引能力的相对大小。以下是几种原子的电负性数值:
| 元素 |
钠 |
镁 |
铝 |
硅 |
| 电负性 |
0.9 |
1.2 |
χ |
1.8 |
①铝的电负性χ的范围是。
②电负性的数值与元素金属性的关系是。
③下列实验能比较镁和铝的金属性强弱的是。
a.测定镁和铝的导电性强弱
b.测定等物质的量浓度的Al2(SO4)3和MgSO4溶液的pH
c.向0.1 mol/LAlCl3和0.1 mol/L MgCl2中加过量NaOH溶液
(3)铝热法是常用的金属冶炼方法之一。
已知:4Al(s)+3O2(g)=2Al2O3(s)ΔH1=-3352 kJ/mol
Mn(s)+O2(g)=MnO2(s)ΔH2= -521 kJ/mol
Al与MnO2反应冶炼金属Mn的热化学方程式是。
(4)冶炼金属铝时,用石墨做电极电解熔融Al2O3。液态铝在(填“阴”或“阳”)极得到,电解过程中,阳极石墨需要不断补充,结合电极反应说明其原因是。
紫外线吸收剂广泛用作有机高分子材料的抗老化剂及化妆品中的防晒剂,其系列产品有许多种类,其中第Ⅰ类产品为二苯甲酮( )及其衍生物,第Ⅱ类为苯甲酸苯酯(
)及其衍生物,第Ⅱ类为苯甲酸苯酯( )的衍生物,某紫外线吸收剂UV-0(属于第Ⅰ类产品)的合成路线如下:
)的衍生物,某紫外线吸收剂UV-0(属于第Ⅰ类产品)的合成路线如下:
已知:

请回答:
(1)A 的结构简式为,③的反应类型为 ;
(2)反应②的化学方程式为;
(3)产物UV-0的同分异构体中,符合第Ⅱ类产品结构的有机化合物共有种;
(4)BAD也是一种紫外线吸收剂,属于第Ⅱ类产品,它的结构简式如下:
BAD中的含氧官能团为(填名称),
1mol BAD最多能和含mol NaOH的溶液进行反应;
(5)BAD 2
2 + M
+ M
M的核磁共振氢谱表明共含有种不同环境的氢;写出含有同样种类的氢且比例关系相同的其中一种同分异构体的结构简式。
开发、使用清洁能源发展“低碳经济”,正成为科学家研究的主要课题。氢气、甲醇是优质的清洁燃料,可制作燃料电池。
(1)已知:① 2CH3OH(1) + 3O2(g) = 2CO2(g) + 4H2O(g) ΔH1 =" –" 1275.6 kJ/mol
② 2CO(g) + O2(g) = 2CO2(g) ΔH2 =" –" 566.0 kJ/mol
③ H2O(g) = H2O(1) ΔH3 =" –" 44.0 kJ/mol
写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式:___________。
(2)生产甲醇的原料CO和H2来源于:CH4(g) + H2O(g)  CO(g) + 3H2(g) ΔH>0
CO(g) + 3H2(g) ΔH>0
①一定条件下CH4的平衡转化率与温度、压强的关系如图a。则Tl ________T2(填“<”、“>”、“=”,下同);A、B、C三点处对应平衡常数(KA、KB、KC)的大小关系为___________。

②100℃时,将1 mol CH4和2 mol H2O通入容积为1 L的定容密封容器中,发生反应,能说明该反应已经达到平衡状态的是__________
a.容器内气体密度恒定
b.单位时间内消耗0.1 mol CH4同时生成0.3 mol H2
c.容器的压强恒定
d.3v正(CH4) = v逆(H2)
如果达到平衡时CH4的转化率为0.5,则100℃时该反应的平衡常数K =___________
(3)某实验小组利用CO(g) 、 O2(g) 、KOH(aq)设计成如图b所示的电池装置,则该电池负极的电极反应式为___________。
X~R是元素周期表中的短周期元素,其性质或结构信息如下表:
| 元素 |
X |
Y |
Z |
W |
R |
| 性质信息 |
能形成+7价的化合物 |
日常生活中常见金属,熔化时并不滴落,好象有一层膜兜着 |
通常状况下能形成短周期中最稳定的双原子分子 |
焰色反应为黄色 |
位于第IVA,是形成化合物种类最多的元素 |
请用化学用语回答下列问题:
(1)X在元素周期表中的位置是_______。
(2)元素W的离子结构示意图为_________。
(3)元素R的最高价氧化物的电子式为_________。
(4)X的氢化物和Z的氢化物反应形成化合物A,A中含有的化学键类型为_________,将A 溶于水,其水溶液中离子浓度由大到小的顺序是_______________ 。
(5)含Y的某化合物可用作净水剂,该物质的水溶液呈酸性,其原因是。(用离子方程式表示)
(6)W的氢氧化物是重要的基本化工原料。写出工业上制取该氢氧化物的离子反应方程式__________ 。