氮化碳是化工行业新合成的一种硬度比金刚石还大的晶体材料,已知在此化合物中各元素均处于其最高或最低价态,据此推断:
(1)氮化碳的化学式可能是__ _ __。
(2)氮化碳的晶体类型为___ _____,该晶体中微粒间的作用力是_ __。
(3)氮化碳晶体可能还具有的性质或特点有_ __。
①熔点很高 ②可以导电 ③不存在单个分子 ④具有空间网状结构
二甲醚是一种重要的清洁燃料,也可替代氟利昂作制冷剂等,对臭氧层无破坏作用。工业上可利用煤的气化产物(水煤气)合成二甲醚。
(1)利用水煤气合成二甲醚的三步反应如下:
① 2H2(g) + CO(g)  CH3OH(g);ΔH =-90.8 kJ·mol-1
CH3OH(g);ΔH =-90.8 kJ·mol-1
② 2CH3OH(g)  CH3OCH3(g) + H2O(g);ΔH=-23.5 kJ·mol-1
CH3OCH3(g) + H2O(g);ΔH=-23.5 kJ·mol-1
③ CO(g) + H2O(g)  CO2(g) + H2(g);ΔH=-41.3 kJ·mol-1
CO2(g) + H2(g);ΔH=-41.3 kJ·mol-1
总反应:3H2(g) + 3CO(g)  CH3OCH3(g) + CO2 (g)的ΔH= ___________;
CH3OCH3(g) + CO2 (g)的ΔH= ___________;
(2)已知反应②2CH3OH(g)  CH3OCH3(g) + H2O(g)某温度下的平衡常数为400 。此温度下,在密闭容器中加入CH3OH,反应到某时刻测得各组分的浓度如下:
CH3OCH3(g) + H2O(g)某温度下的平衡常数为400 。此温度下,在密闭容器中加入CH3OH,反应到某时刻测得各组分的浓度如下:
| 物质 |
CH3OH |
CH3OCH3 |
H2O |
| 浓度/(mol·L-1) |
0.44 |
0.6 |
0.6 |
①比较此时正、逆反应速率的大小:v正 ______ v逆(填“>”、“<”或“=”)。
②若加入CH3OH后,经10 min反应达到平衡,此时c(CH3OH) = _________;该时间内反应速率v(CH3OH) = __________。
(3)在溶液中,反应A+2B C分别在三种不同实验条件下进行,它们的起始浓度均为
C分别在三种不同实验条件下进行,它们的起始浓度均为 、
、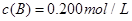 及
及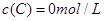 。反应物A的浓度随时间的变化如下图所示。
。反应物A的浓度随时间的变化如下图所示。
请回答下列问题:
与①比较,②和③分别仅改变一种反应条件。所改变的条件和判断的理由是:
②_______________;______________________________________________;
③_______________________________________________;
该反应的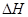 _________0,判断其理由是__________________________________;
_________0,判断其理由是__________________________________;
.丙烷燃烧可以通过以下两种途径:
途径I:4.4g丙烷完全燃烧放出热量为a kJ,写出丙烷燃烧的热化学方程式_________
途径II:等量丙烷按下列反应进行:C3H8(g) ==C3H6(g)+ H2(g)ΔH=+b kJ·mol-1
2C3H6(g)+ 9O2(g) ="=" 6CO2(g) +6H2O(l)ΔH=-c kJ·mol-1
2H2(g)+O2 (g)==2H2O(l)ΔH=-d kJ·mol-1(abcd均为正值)
请回答下列问题:
(1)判断等量的丙烷通过两种途径放出的热量,途径I放出的热量______(填“大于”、“等于”或“小于”)途径II放出的热量。
(2)由于C3H8(g) ==C3H6(g)+ H2(g) 的反应中,反应物具有的总能量______(填“大于”、“等于”或“小于”)生成物具有的总能量,那么在化学反应时。反应物就需要______(填“放出”、或“吸收”)能量才能转化为生成物,因此其反应条件是______________。
(3)b 与a、c、d的数学关系式是______________。
(10分))对于A+2B(气) nC(气)+Q在一定条件下达到平衡后,改变下列条件,请回答:
nC(气)+Q在一定条件下达到平衡后,改变下列条件,请回答:
(1)A量的增减,平衡不移动,则A为______态。
(2)增压,平衡不移动,当n=2时,A的状态为________;当n=3时,A的状态为______。
(3)若A为固体,增大压强,C的组分含量减少,则____。
(4)升温,平衡向右移动,则该反应的逆反应为________反应。
(I)有下列物质:①海水;②氯化钾;③四氧化三铁;④硫磺;⑤铜;⑥水;⑦新鲜的空气;⑧二氧化碳。用序号填写回答:
⑴属于混合物的是___________________;⑵属于单质的是___________________
⑶属于氧化物的是___________________;⑷属于化合物的是___________________
⑸可以导电的是___________________。
(II)下列每组物质中都有一种物质与其他物质在分类上不同,试分析每组物质的组成规律,将这种不同于其他物质的物质找出来,填在后面:
(1)NaCl、KCl、KClO3、BaCl2;
(2)HClO、KClO3、Cl2、NaClO3 ;
(3)H3PO4、NaOH、H2CO3、H2SO4;
(4)空气、N2、HCl气体、CuSO4·5H2O ;
(5)铜、金、汞、钠、铝。
(1)98%的密度为 1. 84 g/cm3的浓硫酸,其物质的量浓度为。若某溶液的密度为ρ g/cm3,物质的量浓度为c mol/L,溶质的摩尔质量为M g/mol,则该溶液的中溶质的质量分数为。
(2)483g Na2SO4·10H2O中所含的Na+的物质的量是,所含H2O分子的数目是,若将其溶于水配成2L溶液,SO42-的物质的量浓度为。