下列离子方程式与所述事实相符且正确的是( )
| A.用硫氰化钾溶液检验溶液中的Fe3+: Fe3++3SCN-=Fe(SCN)3↓ |
| B.钢铁生锈的负极电极反应: Fe —3e—= Fe3+ |
| C.证明氯气氧化性大于硫可用: Cl2+S2-=2Cl-+S↓ |
| D.用钠与硫酸铜溶液反应证明钠的金属性更强: 2Na+Cu2+=Cu+2Na+ |
将高科技用于现代战争,是备受军事专家关注的焦点,让雷达无法侦察到的隐形飞机一直受到全世界的极大关注。用于制造隐形飞机的物质A 具有吸收微波的功能,其主要成分的结构如图,关于该物质的说法正确的是()
| A.该物质属于无机物 |
| B.该物质是一种芳香烃 |
| C.该物质不可能使溴水褪色 |
| D.该物质最多可与3molH2发生加成反应 |
1945年8 月6日和9 日,美国B-29轰炸机在日本广岛、长崎投放的原子弹将两地夷为平地,加速了日本的投降。下列有关化学反应与能量变化的说法中不正确的是()
| A.物质发生化学反应都伴随着能量变化 |
| B.物质发生的变化中伴有能量变化的都是化学变化 |
| C.在一个确定的化学反应关系中,反应物的总能量与生成物的总能量一定不同 |
| D.并不是任何一个化学变化都伴随着能量的放出 |
大理石装修的房屋彰显富丽堂皇,但当食醋不慎滴在大理石地面上时,会使其失去光泽,变得粗糙,下列能正确解释此现象的是()
| A.食醋中的水使碳酸钙溶解 |
| B.食醋中的醋酸将碳酸钙氧化 |
| C.食醋中的醋酸起了催化作用,导致碳酸钙分解了 |
| D.食醋中的醋酸与碳酸钙发生了复分解反应 |
某短周期元素M可用于制造绚丽多彩的焰火,该元素的一个原子可失去2个电子,这2个电子转移到Y元素的2个原子中可形成化合物Z。判断下列说法中,正确的是()
| A.Z属于共价化合物 | B.Z可表示为M2Y |
| C.元素M的最外层电子数多于4个 | D.M形成+2价阳离子 |
雷雨过后,人们感到空气清爽,这是O3的功效。已知该气体在一定条件下会发生如下反应:2O3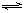 3O2。下列有关叙述中,不正确的是()
3O2。下列有关叙述中,不正确的是()
| A.O2与O3是氧元素的同素异形体 |
| B.曾经风靡一时的致冷剂氟利昂产生的Cl原子是该反应的催化剂,会使该气体分解程度增大 |
| C.阴天时气压增大,O3分解程度会减小 |
| D.气压增大时,O3转化为O2的速率会加快 |