氨气在工农业有着广泛的用途。已知25%氨水的密度为0.91 g/cm3,5%氨水的密度为0.98 g/cm3。
1、(1)配制100mL 2.5mol/L氨水需要浓度为25%氨水______mL(保留2位小数)。
(2)若将上述两溶液等体积混合,所得氨水溶液的质量分数是_____________。
A.等于15% B.大于15% C.小于15% D.无法估算
2、已知:4NH3+O2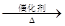 4NO+6NO,4NO+3O2+2H2O
4NO+6NO,4NO+3O2+2H2O 4HNO3
4HNO3
设空气中氧气的体积分数为0.20,氮气的体积分数为0.80。
(1)a mol NO完全转化为HNO3理论上需要氧气_____________mol。
(2)为使NH3恰好完全氧化为NO,氨-空气混合气体中氨的体积分数(用小数表示)为_____________ (保留2位小数)。
(3)20.0 mol NH3用空气氧化,产生混合物的组成为:NO 18.0 mol、O2 12.0 mol、N2 150.0 mol和一定量硝酸,以及其他成分(高温下NO与O2不化合)。计算氨转化为NO和HNO3的转化率。
(4)20.0 mol NH3和一定量空气充分反应后,再转化为硝酸。通过计算,在图中画出HNO3的物质的量n(A)和空气的物质的量n (B)关系的理论曲线。
⑴向NaHSO4溶液中逐滴加入Ba(OH)2溶液至中性,请写出发生反应的离子方程式:___________________________________________________,在以上中性溶液中继续滴加Ba(OH)2溶液,请写出此步反应的离子方程式:______________________________。
⑵向Ba(OH)2溶液中逐滴加入NaHSO4溶液至恰好不再生成沉淀时为止,请写出发生反应的离子方程式:___________________________________________________,在以上溶液中继续滴加NaHSO4溶液,请写出此步反应的离子方程式:________________________。
⑶向Ba(OH)2溶液中逐滴加入明矾[KAl(SO4)2]至溶液中Ba2+恰好完全沉淀,此反应的离子方程式是:,在以上溶液中继续滴加明矾溶液,请写出此步反应的离子方程式:________________________。
某河道旁相邻甲,乙两厂。他们排放的工业废水中,共含有K+、Ag+、Fe3+、Cl-、OH-、NO3 - 六种离子。甲厂的废水明显呈碱性,故甲厂废水中所含有的三种离子是_ _____。
乙厂的废水含有另外三种离子,如果加一定量的_______________(选填活性炭,硫酸亚铁,铁粉),可以回收其中的金属_____________(填金属的元素符号)。转化为沉淀。
经过过滤后的废水主要含有_____________,可用来浇灌农田。
某学生中和滴定实验的过程如下:(a)取一支碱式滴定管,(b)用蒸馏水洗净,(c)即加入待测的 NaOH溶液,(d)记录液面刻度读数,(e)用酸式滴定管精确放出一定量标准酸液,(f)置于未经标准酸液润洗的洁净锥形瓶中,(g)加入适量蒸馏水,(h)加入酚酞试液2滴,(i)滴定时,边滴边摇荡,(j)边注视滴管内液面的变化,(k)当小心滴到溶液由无色变成粉红色时,即停止滴定,(l)记录液面刻度读数,(m)根据滴定管的两次读数得出NaOH深液体积为22mL。指出上述实验过程中的错误之处(用编号表示)___________。
邻-甲基苯甲酸( )多种同分异构体,其中属于酯类,且结构中含有苯环和甲基的同分异构体的结构简式为____、____、_____、____、_____、____(填不满,可以空着)。
)多种同分异构体,其中属于酯类,且结构中含有苯环和甲基的同分异构体的结构简式为____、____、_____、____、_____、____(填不满,可以空着)。
呼吸面具中有Na2O2,可吸收CO2放出O2,若用超氧化钾(KO2)代替Na2O2,也能吸收CO2生成碳酸盐和氧气。
(1)写出KO2与CO2反应的化学方程式___________________________________________。
(2)1 kg Na2O2和1 kg KO2分别和CO2反应生成O2的质量分别为__________________。
(3)你认为选用_____________作为氧化剂更合适。理由是_____________________________。