18世纪,英国国内市场生产的工业产量从基数100增为150,而为出口生产的工业产量从基数100增为550,造成这一现象的主要原因是 ( )
| A.政治上刚刚完成了资产阶级革命,提供了稳定的国内环境 |
| B.英国对外积极开展海外殖民活动,开拓了广阔的海外市场 |
| C.英国已完成工业革命,创造出了前所未有的生产力 |
| D.奴隶贸易提供了大量劳动力,推动英国工业生产进步 |
已知25℃时有关弱酸的电离平衡常数:
| 弱酸化学式 |
CH3COOH |
HCN |
H2CO3 |
| 电离平衡常数(25℃) |
1.8×l0–5 |
4.9×l0–10 |
K1=4.3×l0–7 K2=5.6×l0–11 |
则下列有关说法正确的是
A.等物质的量浓度的各溶液pH关系为:pH(NaCN)>pH(Na2CO3)>pH(CH3COONa)
B.将a mol·L—1 HCN溶液与a mol·L—1 NaOH溶液等体积混合,混合液中:c(OH–)>c(H+),c(Na+)>c(CN–)
C.冰醋酸中逐滴加水,溶液的导电性、醋酸的电离程度、pH均先增大后减小
D.NaHCO3和Na2CO3混合液中,一定有c(Na+)+ c(H+)=c(OH–)+ c(HCO3–) +c(CO32–)[
常温下,将某一元酸HA和NaOH溶液等体积混合,实验信息如下:
| 实验编号 |
c(HA)/mol·L-1 |
c(NaOH) /mol·L-1 |
反应后溶液pH |
| 甲 |
0.1 |
0.1 |
pH= 9 |
| 乙 |
c1[ |
0.2 |
pH=7 |
下列判断不正确的是
A.0.1mol·L-1的HA溶液中由水电离出的c(H+)> 1×10-13mol/L
B.c1一定大于0.2 mol·L-1
C.甲反应后的溶液中:HA占含A-微粒总数的0.01%
D.乙反应后的溶液中:c(Na+) < c(HA) + c(A-)
已知Ksp(BaSO4 )= 1.1×10-10,Ksp(BaCO3)=2.5×10-9。下列说法中正确的是
| A.BaCO3可以转化为BaSO4,反过来则不行 |
| B.BaCO3、BaSO4均不溶于水,所以都可以做钡餐试剂 |
| C.向Na2CO3溶液中加入BaCl2和Na2SO4,当两种沉淀共存时,c(SO42—)/ c(CO32—) = Ksp(BaCO3) / Ksp(BaSO4) |
| D.常温下,BaCO3固体若要在Na2SO4溶液中开始转化为BaSO4,则Na2SO4的浓度须大于2.2×10-6 mol·L-1 |
Mg-H2O2电池可用于驱动无人驾驶的潜航器。该电池以海水为电解质溶液(加入一定量酸),示意图如下。该电池工作时,下列说法正确的是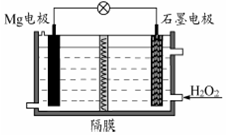
| A.Mg电极是该电池的正极 |
| B.电池总反应为Mg+H2O2+2H+=Mg2++ 2H2O |
| C.电池工作时,石墨周围海水的pH减少 |
| D.电池工作时,溶液中的H+向负极移动 |
X、Y二元素的原子,当它们分别获得两个电子形成稀有气体元素原子层结构时,X放出的热量大于Y放出的热量;Z、W两元素的原子,当它们分别失去一个电子形成稀有气体元素原子的电子层结构时,吸收能量W大于Z。则X、Y和Z、W分别形成的化合物中,离子化合物可能性最大的是
| A.Z2X | B.Z2Y | C.W2X | D.W2Y |