下表是元素周期表的一部分,回答下列有关问题:
| 主族 周期 |
ⅠA |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
0 |
| 2 |
|
|
|
⑤ |
⑦ |
⑧ |
|
|
| 3 |
① |
③ |
④ |
⑥ |
|
⑨ |
⑩ |
|
| 4 |
② |
|
|
|
|
|
|
|
(1)写出⑦单质分子的化学式 ;画出负2价的 ⑨离子结构示意图 ;
写出⑩单质与水反应的离子方程式: 。
(2) ①~⑩元素中最高价氧化物的水化物碱性最强的是________(填化学式)。
①、③、④简单阳离子按离子半径由大到小的顺序排列为_________(用离子符号表示)。
(3)写出①、⑧元素按1:1的原子比例组成的化合物与⑤的最高价氧化物反应的化学方程式: 。
(4) X元素①~⑩元素中的其一种,其氢氧化物既能溶于氢氧化钠溶液中反应,也能与盐酸反应。
则 :X的元素符号是 ,它位于元素周期表的位置 。
X的氢氧化物与盐酸反应的离子方程式 。
(5)①与③化学性质较活泼的是_____,(元素符号)设计实验证明:________________________________________________________________________________________________________(简述实验操作步骤及现象)
可逆反应:2NO2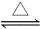 2NO+O2在密闭容器中反应,达到平衡状态的标志是________。
2NO+O2在密闭容器中反应,达到平衡状态的标志是________。
①单位时间内生成n mol O2的同时,生成2n mol NO2
②单位时间内生成n mol O2的同时,生成2n mol NO
③用NO2、NO、O2的物质的量浓度变化表示的反应速率比为2∶2∶1的状态
④混合气体的颜色不再改变的状态
⑤混合气体的密度不再改变的状态
⑥混合气体的平均相对分子质量不再改变的状态
已知向含有Zn2+的溶液中滴加氨水,有白色沉淀Zn(OH)2生成,继续滴加氨水使其过量,沉淀又溶解,生成了[Zn(NH3)4]2+。此外,Zn(OH)2既可溶于盐酸,又可溶于过量的NaOH溶液生成[Zn(OH)4]2-。所以Zn(OH)2是一种两性氢氧化物。现有四组离子,每组有两种金属离子,请各选一种试剂,将它们两者分开,可供选择的试剂有
| A.硫酸 | B.盐酸 |
| C.硝酸 | D.氢氧化钠溶液 |
E.氨水
根据上述内容填写下表:
| 离子组 |
选用试剂(字母代号) |
沉淀物化学式 |
保留在溶液中的离子 |
| ①Zn2+和Al3+ |
|||
| ②Zn2+和Mg2+ |
|||
| ③Zn2+和Ba2+ |
|||
| ④Mg2+和Al3+ |
已知:以铜做催化剂,用空气氧化醇制取醛,事实上是空气先与铜反应生成氧化铜,热的氧化铜再氧化醇生成醛。某实验室中用甲醇、水、空气和铜粉(或氧化铜)制取甲醛溶液。下表给出甲醇、甲醛的沸点和水溶性:
| 沸点/℃ |
水溶性 |
|
| 甲醇 |
65 |
与水混溶 |
| 甲醛 |
-21 |
与水混溶 |
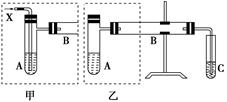
上图是两个同学设计的实验装置,右边的反应装置相同,而左边的气体发生装置不同,分别如甲和乙所示,请回答下列问题:
(1)在仪器组装完成后,加装试剂前必须要进行的操作是______________。
(2)若按甲装置进行实验,则通入A的X是________,B中发生反应的化学方程式为
________________________________________________________________________
________________________________________________________________________。
(3)若按乙装置进行实验,则B管中应装入的物质是________,B中发生反应的化学方程式为________________________________________________________________________
________________________________________________________________________。
(4)试管C中应装入的试剂是
________________________________________________________________________。
(5)两套装置中都需要加热的仪器是________(填A、B或C)。
(6)若欲得到较浓的甲醛溶液,你认为选用哪套装置较好?________(填“甲”或“乙”)。
(7)请设计简单的实验,检验实验后C中所得液体确为甲醛溶液。简述所用试剂、操作、现象及结论。
A、B、C三种物质的化学式都是C7H8O,若滴入FeCl3溶液,只有C呈紫色。若投入金属钠,只有B没有变化。
(1)写出A、B、C的结构简式:A______;B______;C________。
(2)C的另外两种同分异构体的结构简式是①________;②________。
实验室做甲醛和银氨溶液发生银镜反应的实验时:
(1)为产生光亮的银镜,试管应先用________溶液煮沸,倒掉煮沸液后再用清水将试管冲洗干净。
(2)配制银氨溶液时向盛有________溶液的试管中逐滴滴加________溶液,边滴边振荡直到________________________________________________________________________
为止。有关化学反应的离子方程式为:
①________________________________________________________________________。
②________________________________________________________________________。
(3)加热时应用________加热,产生银镜的化学方程式:
________________________________________________________________________。