有一纯净的亚硫酸钠晶体因部分被氧化而变质,为了测定样品中杂质的质量分数进行以下实验过程,按要求填写空格:
(1)向混合溶液中加入的无色溶液A是____________(填化学式),A必须过量的原因是
________________________________________________________________________.
(2)白色沉淀c中含有____________________(填化学式).
(3)无色溶液B通常是_____________(填试剂名称),加入后与c反应的离子方程式为
________________________________________________________________________.
(4)通过以上测定可得到样品中杂质的质量分数的计算式为_______________________.
下图是工业生产硝酸的流程。
合成塔中内置铁触媒,氧化炉中内置Pt-Rh合金网。请回答下列问题:
(1)1909年化学家哈伯在实验室首次合成了氨。2007年化学家格哈德·埃特尔在哈伯研究所证实了氢气与氮气在固体催化剂表面合成氨的反应过程,示意如下:
 分别表示N2、H2、NH3。图⑤表示生成的NH3离开催化剂表面,图②和图③的含义分别是。
分别表示N2、H2、NH3。图⑤表示生成的NH3离开催化剂表面,图②和图③的含义分别是。
(2)合成氨反应的化学方程式为N2(g)+3H2(g) 2NH3(g),写出该反应的化学平衡常数表达式K=
2NH3(g),写出该反应的化学平衡常数表达式K= 。在一定温度和压强下,将H2和N2
。在一定温度和压强下,将H2和N2 按3∶1(体积比)混合后进入合成塔,反应达到平衡时,平衡混合气中NH3的体积分数为15%,此时H2的转化率为。
按3∶1(体积比)混合后进入合成塔,反应达到平衡时,平衡混合气中NH3的体积分数为15%,此时H2的转化率为。
(3)吸收塔中通入空气的目的是。
X、Y、Z、Q、W五种元素的原子序数依次递增。已知: ①W的原子序数为29,其余的均为短周期主族元素;
①W的原子序数为29,其余的均为短周期主族元素;
②X原子的价电子排布为nsnnpn;
③Y元素是空气中含量最多的元素;
④Z元素的电负性大于Y元素,Z原子核外的成对电子数与未成对电子数之比为3:1;
⑤Q元素的电离能数据见下表(单位:kJ/mol)。
| I1 |
I2 |
I3 |
I4 |
I5[] |
...... |
| 578 |
1817 |
2745 |
11575 |
14380 |
...... |







 (1)
(1)





 W元素位于周期表的区,Z2+ 的核外电子排布式是。
W元素位于周期表的区,Z2+ 的核外电子排布式是。
(2)X、Y、Z三种元素的第一电离能数值由小到大的顺序为(用元素符号作答)。
(3)Q元素在周期表中的位置为(填周期数和族序数),它的稳定价态为。
(4)常温下,Y单质的化学性质很稳定,原因是。
(5)X的一种氢化物相对分子质量为26,其中分子中的σ键与π键的键数之比为。
将1 mol I2(g)和2 mol H2置于2L密闭容器中,在一定温度下发生反应:I2(g) + H2(g)
+ H2(g) 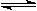 2HI(g);△H<0,并达平衡。HI的体积分数w(HI)随时间变化如图曲线(Ⅱ)所示:
2HI(g);△H<0,并达平衡。HI的体积分数w(HI)随时间变化如图曲线(Ⅱ)所示:
(1)达平衡时,I2(g)的物质的量浓度为;
( 2)若改变反应条件,在甲条件下w(HI)的变化如曲线(Ⅰ) 所示,在乙条件下w(HI)的变化如曲线(Ⅲ) 所示。则甲条件可能是,则乙条件可能是(填入下列条件的序号)
2)若改变反应条件,在甲条件下w(HI)的变化如曲线(Ⅰ) 所示,在乙条件下w(HI)的变化如曲线(Ⅲ) 所示。则甲条件可能是,则乙条件可能是(填入下列条件的序号)
①恒容条件下,升高温度;②恒容条件下,降低温度;
③恒温条件下,缩小反应容器体积;④恒温条件下,扩大反应容器体积;⑤恒温恒容条件下,加入适当催化剂。
(3)若保持温度不变,在另一个相同的2L密闭容器中加入a mol I2(g)、b mol H2(g)和c mol HI(a、b、c均大于0),发生反应,达平衡时,HI的体积分数仍为0.6,则a、b、c的关系是
下图是一个化学过程的示意图。已知甲池的总反应式为:
2CH3OH+3O2+4KOH2K2CO3+6H2O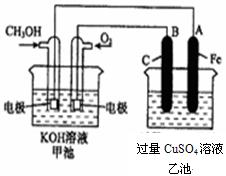
(1)请回答图中,乙电池属于装置,
(2)请回答下列电极的名称:通入CH3OH的电极名称是,B(石墨)电极的名称是。
(3)写出电极反应式:通入CH3OH的电极的电极反应式是。
(4)乙池中反应的化学方程式为。
常温下,0.1mol·L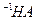 溶液中,
溶液中, =
=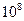 。现取0.1mol·L
。现取0.1mol·L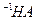 溶液与PH=13的
溶液与PH=13的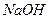 溶液等体积混合(忽略混合后溶液体积的变化)。试回答下列问题:
溶液等体积混合(忽略混合后溶液体积的变化)。试回答下列问题:
(1)混合溶液呈_______性(“酸”﹑“中”或“碱”),理由(用离子方程式表示)________.
(2)混合溶液中由水电离出的 ___________0.1mol·L
___________0.1mol·L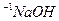 溶液中由水电离出的
溶液中由水电离出的 (填“大于”﹑“小于”或“等于”)。
(填“大于”﹑“小于”或“等于”)。
(3)若混合后溶液的pH=a,则 -
-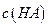 =_________mol·L
=_________mol·L (用含a的代数式表示)。
(用含a的代数式表示)。