已知X、Y、Z为三种原子序数相连的元素,最高价氧化物对应水化物的酸性相对强弱是:HXO4>H2YO4>H3ZO4。则下列说法正确的是
| A.气态氢化物的稳定性:HX>H2Y>ZH3 |
| B.非金属活泼性:Y<X<Z |
| C.原子半径:X>Y>Z |
| D.原子序数:Z>Y>X |
在周期表主族元素中,甲元素与乙、丙、丁三元素相邻,甲、乙的原子序数之和等于丙的原子序数;这四种元素原子的最外层电子数之和为20。下列判断中,正确的是
| A.原子半径:丙>乙>甲>丁 |
| B.气态氢化物的稳定性:甲>丙 |
| C.最高氧化物水化物的酸性:丁>甲 |
| D.乙和甲或乙和丁所能形成的化合物都是有毒物质 |
X、Y、Z 三种元素。已知:X+和Y-两种离子具有相同的电子层结构;Z元素原子核内质子数比Y元素原子核内质子数少9个,Y和Z两元素可以形成42个电子的负一价阴离子。下列有关说法正确的是()
| A.离子半径:X+>Y- |
| B.原子序数Y>X>Z |
| C.X、Y、Z均属于短周期元素 |
| D.X、Y、Z可以形成XYZ、XYZ3、XYZ4等化合物 |
下列说法中正确的是()
①晶体中只要有阳离子,就一定有阴离子
②极性分子中肯定含有极性键,则含有极性键的的分子一定是极性分子
③离子化合物一定含有离子键,则共价化合物中一定不含有离子键
④VIIA族单质从上到下,熔沸点越来越高,则IA族单质的熔沸点也越来越高
⑤H2O分子间存在着氢键,故H2O分子比H2S分子稳定
⑥在熔融状态和水溶液中均不能导电的物质称为非电解质
⑦HClO4酸性比H2SO4酸性强,说明氯的非金属性比硫强
| A.①②③⑤ | B.②④⑥ | C.③⑦ | D.①③⑥ |
将1 mol H2(g)和2 mol I2(g)置于某2L密闭容器中,在一定温度下发生如下反应,并达到平衡:H2(g)+I2(g)  2HI(g);ΔH<0。HI的体积分数ω(HI)随时间变化如图(Ⅰ)所示,若改变反应条件,ω(HI)的变化曲线如图(Ⅱ)所示,则改变的条件可能是( )
2HI(g);ΔH<0。HI的体积分数ω(HI)随时间变化如图(Ⅰ)所示,若改变反应条件,ω(HI)的变化曲线如图(Ⅱ)所示,则改变的条件可能是( )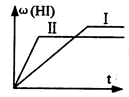
| A.恒温条件下,加入适当催化剂 |
| B.恒温条件下,缩小反应容器体积 |
| C.恒容条件下升高温度 |
| D.恒温条件下,扩大反应容器体积 |
在体积不变的密闭容器中,在一定条件下发生下列反应:2A B(g)+C(s),达到平衡后,升高温度使容器内气体的密度增大,则下列叙述中正确的是( )
B(g)+C(s),达到平衡后,升高温度使容器内气体的密度增大,则下列叙述中正确的是( )
| A.若正反应为吸热反应,则A为非气体 |
| B.若正反应为放热反应,则A为非气体 |
| C.在平衡体系中加入少量的C,该平衡向逆反应方向移动 |
| D.改变压强对该平衡的移动无影响 |