某同学为测定10g某赤铁矿石中氧化铁的质量分数,利用稀硫酸和锌粒制取氢气,设计了下图所示的装置,进行有关的实验探究(提示:3H2+Fe2O3 2Fe+3H2O;杂质不参加反应,假定每步均完全反应或吸收)。请回答有关问题:
2Fe+3H2O;杂质不参加反应,假定每步均完全反应或吸收)。请回答有关问题: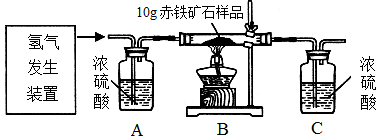
得到如下数据:
| 装置 |
B |
C |
| 反应前质量 |
84.3g |
294.1g |
| 反应后质量 |
81.9g |
296.8g |
(1)请计算该赤铁矿石样品中氧化铁的质量分数。(写出计算过程)
(2)该实验还可测定组成水中各元素之间的质量关系,请用表中实验数据列式表示出水中氢、氧元素的质量比为_______________________________________________(只列式,不计算);若玻璃管中的氧化铁没有完全反应,则求得水中氢、氧元素的质量比会__________(选填“偏大”、“偏小” 或“不变”)。
构建知识网络是一种重要的学习方法。图为某校化学学习小组的小阳同学绘制的铁的化学性质网络示意图。请分析回答下列问题:

(1)反应①中可用 ▲(填化学式)作还原剂;
⑵写出高炉中发生的反应①的化学方程
式: ▲;
写出反应③的化学方程式 ▲;
⑶反应②导致每年有大量的钢铁锈蚀,为阻止该反应的发生,人们常采用在钢铁表面涂刷油漆或镀上其它金属等方法。这两种方法的共同原理是阻止钢铁
与 ▲接触;
⑷该化学学习小组为了分析生铁中铁的含量,进行了如下实验研究:取12g生铁与10%的盐酸反应,并绘制了加入盐酸质量与放出气体质量的关系图(见右下图)。(说明:生铁中杂质不溶于水,不与盐酸、硫酸铜溶液反应。)
①铁完全反应用去盐酸的质量为 ▲g。
②生铁中铁的质量分数为多少?(写出计算过程,结果保留到小数点后一位)
▲
(5)某同学列出了如下计算式:
生铁与盐酸刚好反应完全时所得溶液质量= (146+12-a)g
小明对该计算式提出了质疑,请指出其中的错误 ▲
。
(6)小华另设计了一个实验方案:用12g生铁粉与20%的硫酸铜溶液反应来分析生铁中铁的含量。请你画出加入硫酸铜溶液质量与固体质量变化关系的曲线。
小苏打(NaHCO3)是食品工业中一种应用最广泛的疏松剂。资料显示,固态小苏打50℃以上或在潮湿的空气中开始逐渐分解生成碳酸钠、二氧化碳和水,270℃时完全分解。
(1)小苏打、纯碱、烧碱都是化工生产常用试剂,水溶液均显碱性,从物质分类角度看不属于盐的是▲(填写化学式),小苏打的保存应注意▲。
(2)小苏打(NaHCO3)和纯碱中含钠元素质量分数较大的是▲(填写化学式)。
(3)某化学兴趣小组同学为了对在干燥空气中久置的小苏打样品进行分析,称取一份31.4 g混合均匀的样品,用酒精灯对其充分加热,收集到干燥的CO2气体3.3 g。通过计算判断该小苏打样品是否变质,如果变质计算该样品中NaHCO3质量分数是多少?
氢化钙(CaH2)是一种重要的制氢剂,与水接触时发生如下反应:
CaH2+2H2O = Ca(OH) 2+2H2↑。若要制得2 g氢气,需CaH2的质量为多少?
有两种外观类似黄金的合金①Cu-Zn和②Cu-Ag,若实验室只提供一瓶稀硫酸和必要的仪器。
(1)你认为能测出合金(填序号)中铜的质量分数;
(2)取上述(1)中合金粉末20g放入烧杯中,加入50g稀硫酸,恰好完全反应,测得烧杯内剩余物质的质量为69.8g。
求:①产生氢气的质量;②求出该合金中铜的质量分数。
环保部门对某工厂的废水进行抽样分析,结果表明废水中含少量硫酸。取一定量废水用质量分数为2%的氢氧化钠溶液中和(已知废水中的其它成分不与氢氧化钠反应),至pH = 7时,消耗氢氧化钠溶液的质量为40g,同时测得反应后溶液质量为138g。请计算该工厂排放的废水中硫酸的质量分数。