在10L密闭容器中,A、B、C三种气态物质构成可逆反应体系,其关系如图所示。下列说法错误的是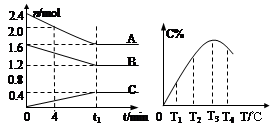
A.0~4分钟时,A的平均反应速率为0.01mol·L-1·min-1
B.由T1向T2变化时,V正>V逆
C. 此反应的正反 应为吸热反应
D.其它条件不变,加压,达新平衡时,C的体积分数增大
下列化合物的核磁共振氢谱中出现三组峰的是
| A.2,2,3,3一四甲基丁烷 | B.2,3,4一三甲基戊烷 |
| C.3,4一二甲基己烷 | D.2,5一二甲基己烷 |
下列叙述错误的是
| A.用金属钠可区分乙醇和乙醚 |
| B.用高锰酸钾酸性溶液可区分乙烷和3-乙烯 |
| C.用水可区分苯和溴苯 |
| D.用新制的银氨溶液可区分甲酸甲酯和乙醛 |
下列说法不正确的是
| A.麦芽糖及其水解产物均能发生银镜反应 |
| B.用溴水即可鉴别苯酚溶液、2,4-已二烯和甲苯 |
| C.在酸性条件下,CH3CO18OC2H5的水解产物是CH3CO18OH和C2H5OH |
| D.用甘氨酸和丙氨酸缩合最多可形成4种二肽 |
下列有机物命名正确的是
A.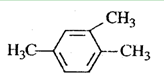 1,3,4-三甲苯 1,3,4-三甲苯 |
B.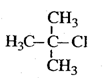 2-甲基-2-氯丙烷 2-甲基-2-氯丙烷 |
C.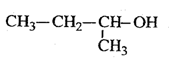 2-甲基-1-丙醇 2-甲基-1-丙醇 |
D.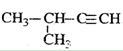 2-甲基-3-丁炔 2-甲基-3-丁炔 |
下列对有机物结构或性质的描述,错误的是
| A.一定条件下,Cl2可在甲苯的苯环或侧链上发生取代反应 |
| B.苯酚钠溶液中通入CO2生成苯酚,则碳酸的酸性比苯酚弱 |
| C.乙烷和丙烯的物质的量各1mol,完成燃烧生成3molH2O |
| D.光照下2,2—二甲基丙烷与Br2反应其一溴取代物只有一种 |