某校化学研究性学习小组欲设计实验验证Al、Fe、Cu的金属活动性,他们提出了以下两种方案。请你帮助他们完成有关实验项目:
(1)用三种金属与盐酸反应的现象来判断,实验中除选择大小相同的金属片外,还需要控制
_____________ 、_____________ 相同;若选用一种盐溶液验证三种金属的活泼性,该试剂为 。
(2)①若用Fe、Cu作电极设计成原电池,以确定Fe、Cu的活动性。试在下面方框中画出原电池装置图,标出原电池的电极材料和电解质溶液。
上述装置中正极反应式为 。
②某小组同学采用Al、Fe作为电极,只用一个原电池证明三种金属的活动性,则电解质溶液最好选用 。
| A.0.5 mol·L-1氯化亚铁溶液 | B.0.5 mol·L-1氯化铜溶液 |
| C.0.5 mol·L-1盐酸 | D.0.5 mol·L-1氯化亚铁和0.5 mol·L-1氯化铜混合溶液 |
(3)利用提供的试剂和用品:0.1 mol·L-1盐酸溶液、0.1 mol·L-1醋酸溶液、0.5 mol·L-1氯化铝溶液、0.5 mol·L-1氢氧化钠溶液、PH试纸。
请设计最简单实验证明氢氧化铝为弱碱
下图是某化工厂对海水资源的综合利用的示意图。
(1)目前国际上实用的“海水淡化”主要技术之一是蒸馏法。蒸馏法是将海水变成蒸汽,蒸汽经过冷却而得高纯度淡水,由此可判断蒸馏法是:(填物理变化、化学变化)
(2)工业上利用电解饱和食盐水可制得重要化工产品,又称为“氯碱工业”。电解饱和食盐水的离子方程式为:。阳极产生气体的如何检验。利用电解所得气体制36.5%的浓盐酸100t,最少需要消耗食盐:t。
(3)分离出粗盐的母液中含有Mg2+,从图中可看出对母液进行一系列的加工可制得金属镁。
①在母液中加入石灰乳所起的作用是:。
②从充分利用当地海洋化学资源,就地取材,经济效益的角度考虑,生产生石灰的原料可是:。
③电解熔融氯化镁的化学方程式是:。
④氮气和氩是两种化学性质相对稳定的气体,都可用做白炽灯的填充气体。但工业上冷却电解无水氯化镁所得的镁蒸气时,却选择稀有气体氩。试用化学反应方程式解释不选用氮气的原因:。
实验室用密度为1.18g/mL,质量分数为36.5%浓盐酸配制250mL0.1mol/L的盐酸溶液,填空并请回答下列问题:
(1)配制250mL0.1mol/L的盐酸溶液需要浓盐酸的体积为mL除了烧杯和量筒还需要的仪器有
(2)配制时,其正确的操作顺序是(用字母表示,每个字母只能用一次)。
| A.用30mL水洗涤烧杯2—3次,洗涤液均注入容量瓶,振荡 |
| B.用量筒准确量取所需的浓盐酸的体积,沿玻璃棒倒入烧杯中,再加入少量水(约30mL),用玻璃棒慢慢搅动,使其混合均匀 |
| C.将已冷却的盐酸沿玻璃棒注入250mL的容量瓶中 |
| D.将容量瓶盖紧,振荡,摇匀 |
E.改用胶头滴管加水,使溶液凹面恰好与刻度相切
F.继续往容量瓶内小心加水,直到液面接近刻线2—3 cm处
(3)操作A中,将洗涤液都移入容量瓶,其目的是。
(4)若出现如下情况,对所配溶液浓度将有何影响?
加蒸馏水时不慎超过了刻度;定容时俯视_________________________。
(8分)实验室常用氧化浓盐酸的方法制取氯气,课本中实验装置如下图: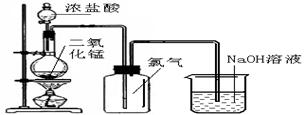
⑴写出制氯气的化学方程式:,
⑵甲同学认为该装置制得的氯气不纯,在收集氯气之前补充了下面实验装置,你认为如何连接(用ABCD字母连接):。浓硫酸的作用,
饱和食盐水的作用是。
(6分)右图所示装置有多种用途,请回答下列问题: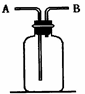
(1)检验:证明CO中混有CO2,装置内应盛
(2)集气:若用排空气法收集比空气轻的气体时,气体应从装置的端通入(填A或B,下同);若收集比空气重的气体,则气体从端通入。
(10分)欲用含有少量氯化钙的氯化钠固体,配制100 mL 1mol/L的氯化钠溶液,设计了下面的操作方案。根据方案操作步骤回答下列问题: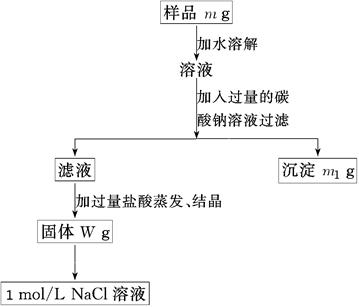
⑴称量粗盐样品m g,样品放在托盘天平左盘上。
⑵过滤时,需用到的玻璃仪器除烧杯、玻璃棒外有。
⑶蒸发操作时应将液体放在______中加热,等加热至________时即停止加热。
⑷在样品的溶液中加入过量的Na2CO3溶液,作用是____________________________,反应的离子方程式是______________________。
⑸在滤液中加入盐酸的作用是________________,发生反应的化学方程式是___________。
⑹配制100 mL 1mol/L的NaCl溶液时,应从W g固体中称取NaCl的质量为____________。