下列操作中,能使电离平衡H2O H++OH-,向右移动且溶液呈酸性的是( )
H++OH-,向右移动且溶液呈酸性的是( )
| A.向水中加入NaHSO4溶液 | B.向水中加入Al2(SO4)3固体 |
| C.向水中加入Na2CO3溶液 | D.将水加热到100℃,使pH=6 |
下列叙述正确的是
| A.发生化学反应时失去电子越多的金属原子,还原能力越强 |
| B.金属阳离子被还原后,一定得到该元素的单质 |
| C.核外电子总数相同的原子,一定是同种元素的原子 |
| D.能与酸反应的氧化物,一定是碱性氧化物 |
可逆反应N2(g)+3H2(g)  2NH3(g)的正、逆反应速率可用各反应物或生成物浓度的变化来表示。下列各关系中能说明反应已达到平衡状态的是
2NH3(g)的正、逆反应速率可用各反应物或生成物浓度的变化来表示。下列各关系中能说明反应已达到平衡状态的是
| A.3v正(N2)=v正(H2) | B.v正(N2)=v逆(NH3) |
| C.v正(N2)=3v逆(H2) | D.2v正(H2)=3v逆(NH3) |
下列说法不正确的是
| A.凡是铵盐都能与苛性钠共热产生NH3 |
| B.NH4HCO3受热分解产生的气体经足量碱石灰干燥后可得到纯净的氨气 |
| C.N2与O2在放电条件下化合属于氮的固定 |
| D.工业硝酸略显黄色是由于里面含有Fe3+的缘故 |
下列物质在固体状态时,所有原子的最外层都满足8电子结构且属于分子晶体的是
| A.NH4Cl | B.H2O | C.SiO2 | D.PCl3 |
某粒子用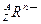 表示。下列关于该粒子的叙述正确的是
表示。下列关于该粒子的叙述正确的是
| A.所含质子数=A-n | B.所含电子数=Z+n |
| C.所含中子数=A-Z+n | D.该粒子所含质子数一定多于中子数 |