海洋植物如海带、马尾藻等含有丰富的碘元素,实验室从海带中提取碘的流程如下:
(1)提取碘的过程中有关实验的操作名称① ② ③ ④
(2)写出过程②中有关反应的离子方程式 ;
该反应中氧化剂是 ,氧化产物是 。
(3)提取碘的过程中,可选择得有机试剂是 ;
| A.酒精 | B.水 | C.四氯化碳 | D.甘油 |
在碘水中加入上述有机试剂,振荡静置,可观察到的现象是
有A、B、C、D四种元素,其中A元素和B元素的原子都有1个未成对电子,A+比B-少一个电子层,B原子得一个电子后3p轨道全满;C原子的p轨道中有3个未成对电子,其气态氢化物在水中的溶解度是同族元素所形成的氢化物中最大的;D的最高化合价和最低化合价的代数和为4,其最高价氧化物中含D的质量分数为40%,且其核内质子数等于中子数。R是由A、D两元素形成的离子化合物,其中A与D离子数之比为2∶1。请回答下列问题: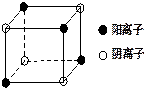
⑴A单质、B单质、化合物R的熔点大小顺序为下列的(填序号):
①A单质>B单质>R; ②R>A单质>B单质;
③B单质>R >A单质; ④A单质>R>B单质。
⑵在CB3分子中C元素原子的原子轨道发生的是________杂化,其固体的晶体类型为;
⑶写出D原子的核外价电子排布式_,C的氢化物比D的氢化物在水中溶解度大得多的可能原因
;
⑷右图是D和Fe形成的晶体FeD2最小单元“晶胞”,FeD2晶体
中阴、阳离子数之比为,FeD2物质中具有的化
学键类型为。
联氨(N2H4)是一种无色可燃的弱碱性液体,是液体大推力火箭常用的高能燃料。
⑴已知联分子中的N原子最外层满足8电子相对稳定结构,则下列说法正确的是
| A.联氨(N2H4)结构与C2H4相似,存在N=N双键 | |
| B.一分子联氨中含有的电子对数目为5 |
C.联氨中的N原子的杂化类型为sp3杂化 |
| D.联氨能与HCl发生化合反应生成N2H6Cl2 |
⑵联氨可以采用尿素[CO(NH2)2]为原料制取,方法是在高锰酸钾催化剂存在下,尿素和次氯酸钠、氢氧化钠溶液反应生成联氨、另外两种正盐和水,写出其反应的化学方程式;
⑶火箭推进器中分别装有联氨和过氧化氢,当它们混合时即产生气体,并放出大量热。已知:12.8 g液态联氨与足量过氧化氢反应生成氮气和水蒸气,放出256.65 kJ的热量,写出该反应的热化学方程式 。
氢溴酸在医药和石化工业上有广泛用途。下图是模拟工业制备氢溴酸粗品并精制的流程:
根据上述流程回答下列问题: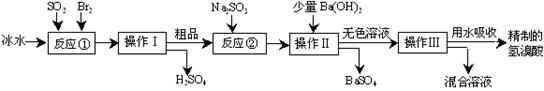 ⑴反应①中发生反应的化学方程式为;
⑴反应①中发生反应的化学方程式为;
⑵反应①中使用冰水的目的是;
⑶操作Ⅱ和操作Ⅲ的名称分别是、;
⑷反应②中加入Na2SO3的目的是;
⑸上述流程中制得的氢溴酸往往带有淡淡的黄色。请设计简单实验加以探究(包含提出假设,然后进行验证的过程)。
。
某课外小组设计的实验室制取乙酸乙酯的装置(如图所示),A中放有浓硫酸,B中放有乙醇、无水醋酸,D中放有饱和碳酸钠溶液。按图连接装置,用酒精灯对烧瓶B加热,当观察到D中有明显现象时停止实验。试完成下列问题
(1)在烧瓶中除了加入乙醇、浓硫酸和乙酸外,还应放入几块碎瓷片,其目的是:_________。
(2)球形干燥管除起冷凝作用外,另一重要作用是_________________。
(3)装置D中饱和碳酸钠溶液的作用是___________________________
(4)在该实验中,若用1mol乙醇和1mol 乙酸在浓硫酸作用下加热,充分反应,能否生成1mol乙酸乙酯?,原因是:。
某化学研究性学习小组通过查阅资料,设计了如下图所示的方法以含镍废催化剂为原料来制备NiSO4•7H2O。已知某化工厂的含镍催化剂主要含有Ni,还含有Al(31%)、Fe(1.3%)的单质及氧化物,其他不溶杂质(3.3%)。
部分阳离子以氢氧化物形式完全沉淀时的pH如下:
| 沉淀物 |
Al(OH)3 |
Fe(OH)3 |
Fe(OH)2 |
Ni(OH)2 |
| pH |
5.2 |
3.2 |
9.7 |
9.2 |
回答下列问题:
⑴操作a、c中需使用的仪器除铁架台(带铁圈)、酒精灯、烧杯、玻璃棒外还需要的主要仪器为。
⑵“碱浸”过程中发生的离子方程式是。
⑶“酸浸”时所加入的酸是 (填化学式)。酸浸后,经操作a分离出固体①后,溶液中可能含有的金属离子是。
⑷操作b为调节溶液的pH,你认为pH的最佳调控范围是。
⑸“调pH为2~3”的目的是。
⑹产品晶体中有时会混有少量绿矾(FeSO4·7H2O),其原因可能是。